 | |
| Имена | |
|---|---|
| Название IUPAC Цианид меди (I) | |
| Другие названия Цианид меди, цианид меди, куприцин | |
| Идентификаторы | |
| Номер CAS | |
| 3D-модель (JSmol ) | |
| ChemSpider | |
| ECHA InfoCard | 100.008.076 |
| Номер EC |
|
| PubChem CID | |
| Номер RTECS |
|
| UNII | |
| Номер ООН | 1587 |
| CompTox Dashboard (EPA ) | |
InChI
| |
УЛЫБКИ
| |
| Свойства | |
| Химическая формула | CuCN |
| Молярная масса | 89,563 г / моль |
| Внешний вид | грязно-белый / бледно-желтый порошок |
| Плотность | 2,92 г / см |
| Температура плавления | 474 ° C (885 ° F; 747 K) |
| Растворимость в воде | незначительная |
| Растворимость | нерастворим в этаноле, холодных разбавленных кислотах ;. растворим в NH4OH, KCN и DMF |
| Магнитная восприимчивость (χ) | -24,0 · 10 см / моль |
| Структура | |
| Кристаллическая структура | моноклинический |
| Опасности | |
| Паспорт безопасности | Оксфордский паспорт безопасности |
| Пиктограммы GHS |   |
| Сигнальное слово GHS | Опасно |
| Предупреждения об опасности GHS | H300, H310, H330, H400, H410 |
| Меры предосторожности GHS | P260, P262, P264, P270, P271, P273, P280, P284, P301 + 310, P302 + 350, P304 + 340, P310, P320, P321, P322, P330, P361, P363, P391, P403 + 233, P405, P501 |
| NFPA 704 (огненный алмаз) |  0 4 0 0 4 0 |
| Температура воспламенения | Невоспламеняющийся |
| NIOSH (воздействие на здоровье США пределы): | |
| PEL (Допустимое) | TWA 1 мг / м (как Cu) |
| REL (Рекомендуемое) | TWA 1 мг / м (как Cu) |
| IDLH (Непосредственная опасность) | TWA 100 мг / м (как Cu) |
| Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |
| ink ссылки | |
Цианид меди (I) представляет собой неорганическое соединение с формулой CuCN. Это не совсем белое твердое вещество встречается в двух полиморфных модификациях ; Загрязненные образцы могут быть зелеными из-за присутствия примесей Cu (II). Соединение может быть использовано в качестве катализатора, при гальванике меди и в качестве реагента при получении нитрилов.
Цианид меди является координационным полимером. Он существует в двух полиморфных модификациях, каждый из которых содержит - [Cu-CN] - цепи, состоящие из линейных центров меди (I), связанных цианидными мостиками. В высокотемпературном полиморфе HT-CuCN, который изоструктурен AgCN, линейные цепи упаковываются на гексагональной решетке, а соседние цепи смещены на +/- 1/3 c, рис. 1. В В низкотемпературном полиморфе LT-CuCN цепи отклоняются от линейности и упаковываются в волнистые слои, которые упаковываются в виде AB с цепями в соседних слоях, повернутых на 49 °, Рисунок 2.
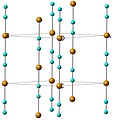
Рисунок 1: Структура HT- CuCN показывает цепи, идущие вдоль оси c. Обозначения: медь = оранжевый и голубой = неупорядоченные цианидные группы "голова к хвосту".

Фиг. 2: Структура LT-CuCN, показывающая листы цепочек, уложенных друг на друга в стиле ABAB. Ключевые медь = оранжевый и голубой = неупорядоченные цианидные группы голова к хвосту.
LT-CuCN можно превратить в HT-CuCN путем нагревания до 563 К в инертной атмосфере. В обоих полиморфах длины связей меди с углеродом и меди с азотом составляют ~ 1,85 Å, а мостиковые цианидные группы демонстрируют разупорядочение от головы к хвосту.
Цианид меди имеется в продаже и поставляется как низкотемпературный полиморф. Его можно получить восстановлением сульфата меди (II) гидросульфитом натрия при 60 ° C с последующим добавлением цианида натрия для осаждения чистого LT-CuCN в виде бледно-желтого цвета. порошок.
При добавлении бисульфита натрия раствор сульфата меди меняет цвет с синего на зеленый, после чего добавляется цианид натрия. Реакция проводится в умеренно кислых условиях. Цианид меди исторически получали обработкой сульфата меди (II) цианидом натрия, в этой окислительно-восстановительной реакции цианид меди (I) образуется вместе с дицианом :
Поскольку этот способ синтеза дает дициан, использует два эквивалента цианида натрия на эквивалент произведенного CuCN, и полученный цианид меди нечистый, это не промышленное производство метод. Сходство этой реакции с реакцией между сульфатом меди и иодидом натрия с образованием иодида меди (I) является одним из примеров цианид-ионов, действующих как псевдогалогенид. Это также объясняет, почему цианид меди (II) Cu (CN) 2 не был синтезирован.
Цианид меди нерастворим в воде, но быстро растворяется в растворах, содержащих CN, с образованием [Cu (CN) 3 ] и [Cu (CN) 4 ], которые демонстрируют тригональную плоскую и тетраэдрическую координационную геометрию соответственно. Эти комплексы контрастируют с комплексами цианидов серебра и золота, которые образуют ионы [M (CN) 2 ] в растворе. Координационный полимер KCu (CN) 2 содержит [Cu (CN) 2 ] звеньев, которые связываются вместе, образуя спиральные анионные цепи.
Цианид меди также растворим в концентрированный водный аммиак, пиридин и N-метилпирролидон.
Цианид меди используется для гальваники меди.
CuCN - важный реагент в химии медьорганических соединений. Он реагирует с литийорганическими реагентами с образованием «смешанных купратов» с формулами Li [RCuCN] и Li 2[R2CuCN]. Использование CuCN произвело революцию в использовании более простых медьорганических реагентов типа CuR и LiCuR 2, реагентов Гилмана. В присутствии цианида эти смешанные купраты легче очищаются и более стабильны.
Смешанные купраты Li [RCuCN] и Li 2[R2CuCN] действуют как источники карбанионов R, но с меньшей реакционной способностью по сравнению с исходным литийорганическим реагентом. Таким образом, они полезны для сопряженных добавлений и некоторых реакций замещения. Добавление CuCN к
CuCN также образует силильные и станнильные реагенты, которые используются в качестве источников R 3 Si и R 3 Sn.
CuCN используется для превращения арилгалогенидов в нитрилы.
| На Викискладе есть материалы, связанные с цианидом меди (I). |