 | |
 | |
| Имена | |
|---|---|
| Название IUPAC Карбонат кобальта (II) | |
| Другие названия Карбонат кобальта; соль кобальта (II) | |
| Идентификаторы | |
| Номер CAS |
|
| 3D-модель (JSmol ) | |
| ChemSpider | |
| ECHA InfoCard | 100.007.428 |
| PubChem CID | |
| UNII |
|
| CompTox Dashboard (EPA ) | |
InChI
| |
УЛЫБАЕТСЯ
| |
| Свойства | |
| Химическая формула | CoCO 3 |
| Молярная масса | 118,941 г / моль |
| Внешний вид | красные / розовые кристаллы ( безводный). розовый, фиолетовый, красный кристаллический порошок (гексагидрат) |
| Плотность | 4,13 г / см |
| Точка плавления | 427 ° C (801 ° F; 700 K). разлагается до плавление до оксида кобальта (II) (безводного). 140 ° C (284 ° F; 413 K). разлагается (гексагидрат) |
| So смазываемость в воде | Карбонат кобальта (II) не растворяется в дистиллированной воде. |
| Произведение растворимости (Ksp) | 1,0 · 10 |
| Растворимость | растворим в кислоте. незначительно в спирте, метилацетат. не растворим в этанол |
| Показатель преломления (nD) | 1,855 |
| Структура | |
| Кристаллическая структура | Ромбоэдрический (безводный). Тригональный (гексагидрат) |
| Термохимия | |
| Стандартная молярная. энтропия ( S 298) | 79,9 Дж / моль · K |
| Стандартная энтальпия образования. (ΔfH298) | −722,6 кДж / моль |
| свободная энергия Гиббса (ΔfG˚) | -651 кДж / моль |
| Опасности | |
| Пиктограммы GHS |   |
| Сигнальное слово GHS | Предупреждение |
| Краткая характеристика опасности GHS | H302, H315, H317, H319, H335, H351 |
| Меры предосторожности GHS | P261, P280, P305 + 351 + 338 |
| NFPA 704 (огненный ромб) |  0 2 0 0 2 0 |
| Смертельная доза или концентрация (LD, LC): | |
| LD50(средняя доза ) | 640 мг / кг (перорально, крысы) |
| Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки в ink | |
Карбонат кобальта (II) представляет собой неорганическое соединение с формулой CoCO 3. Это красноватое парамагнитное твердое вещество является промежуточным продуктом гидрометаллургической очистки кобальта из его руд. Это неорганический пигмент и предшественник катализаторов. Карбонат кобальта (II) также встречается в виде редкого красно-розового минерала сферокобальтит.
Его получают путем объединения растворов сульфата кобальта и бикарбоната натрия :
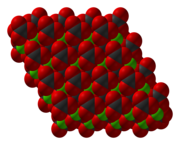
CoCO 3 имеет структуру, подобную кальцит, состоящий из кобальта с октаэдрической координационной геометрией.
Нагревание карбоната протекает типичным для кальцинирования, за исключением того, что материал частично окисляется:
Полученный Co3O4 обратимо превращается в CoO при высоких температурах. Как и большинство карбонатов переходных металлов, карбонат кобальта нерастворим в воде, но легко разрушается минеральными кислотами:
Он используется для получения многих координационных комплексов. Реакция карбоната кобальта (II) и ацетилацетона в присутствии перекись водорода дает трис (ацетилацетонато) кобальт (III). Эти комплексы являются хиральными и часто могут быть разделены на отдельные энантиомеры.
карбонат кобальта является предшественником карбонила кобальта и различных солей кобальта. Он является компонентом диетических добавок, поскольку кобальт является важным элементом. Он является предшественником голубой керамики. глазури, как известно, в случае фаянсовой посуды.
Умеренно редкий сферокобальтит представляет собой естественную форму карбоната кобальта, причем хорошие образцы поступают особенно из Республика Конго. Это кобальтофобный кальциевый разновидность, которая по привычке очень похожа на сферокобальтит.
Соединение вредно при проглатывании и раздражает глаза и кожу.