Хлорамфениколацетилтрансфераза
редактировать
Хлорамфениколацетилтрансфераза (или CAT ) представляет собой бактериальный фермент (EC 2.3.1.28 ), который выводит токсины на антибиотик хлорамфеникол и отвечает за хлорамфеникол устойчивость у бактерий. Этот фермент ковалентно присоединяет ацетил группу ацетил-КоА к хлорамфениколу, что предотвращает связывание хлорамфеникола с рибосомами. Остаток гистидина, расположенный в С-концевой части фермента, играет центральную роль в его каталитическом механизме.
Была определена кристаллическая структура фермента типа III из Escherichia coli со связанным хлорамфениколом. CAT представляет собой тример из идентичных субъединиц (мономер Mr 25000), и тримерная структура стабилизируется рядом водородных связей, некоторые из которых приводят к протяжению бета-слоя через границу раздела субъединиц. Хлорамфеникол связывается в глубоком кармане, расположенном на границе между соседними субъединицами тримера, так что большинство остатков, образующих связывающий карман, принадлежат одной субъединице, в то время как каталитически важный гистидин принадлежит соседней субъединице. His195 имеет подходящее положение, чтобы действовать в качестве основного основного катализатора в реакции, а требуемая таутомерная стабилизация обеспечивается необычным взаимодействием с карбонильным кислородом основной цепи.
Применение
Используется CAT в качестве репортерной системы для измерения уровня промотора или его тканеспецифической экспрессии. Анализ CAT включает мониторинг ацетилирования радиоактивно меченного хлорамфеникола на планшете TLC ; Активность CAT определяется путем поиска ацетилированных форм хлорамфеникола, которые имеют значительно более высокую скорость миграции по сравнению с неацетилированной формой.
Ссылки
Эта статья включает текст из общественного достояния
Pfam и
InterPro :
IPR001707
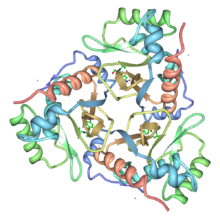 Ленточная диаграмма тримера хлорамфениколацетилтрансферазы со связанным хлорамфениколом. Из PDB : 3CLA .
Ленточная диаграмма тримера хлорамфениколацетилтрансферазы со связанным хлорамфениколом. Из PDB : 3CLA .