 . Cd3As2с ориентацией (112) и (400) . Cd3As2с ориентацией (112) и (400) | |
 . STM изображение (112) поверхность . STM изображение (112) поверхность | |
| Имена | |
|---|---|
| Другие имена Диарсенид трикадмия | |
| Идентификаторы | |
| Номер CAS | |
| 3D-модель (JSmol ) | |
| ChemSpider | |
| ECHA InfoCard | 100.031.336 |
| Номер EC |
|
| PubChem CID | |
| Панель управления CompTox (EPA) | |
InChI
| |
УЛЫБКИ
| |
| Свойства | |
| Химическая формула | Cd3As2 |
| Молярная масса | 487,08 г / моль |
| Внешний вид | твердое вещество, темно-серый |
| Плотность | 3,031 |
| Температура плавления | 716 ° C (1321 ° F; 989 K) |
| Растворимость в воде | разлагается в воде |
| Структура | |
| Кристаллическая структура | Тетрагональная, tI160 |
| Пространственная группа | I41cd, № 110 |
| Решетка константа | a = 1,26512 (3) нм, c = 2,54435 (4) нм |
| Опасности | |
| Пиктограммы GHS |     |
| Сигнальное слово GHS | Опасность |
| Краткая характеристика опасности GHS | H301, H312, H330, H350, H400, H410 |
| Меры предосторожности GHS | P201, P202, P260, P261, P264, P270, P271, P273, P280, P281, P284, P301 + 310, P302 + 352, P304 + 340, P308 + 313, P310, P311, P312, P320, P321, P322, P330, P363, P391, P403 + 233 |
| NFPA 704 (огненный алмаз) |  1 4 0 1 4 0 |
| Смертельная доза или концентрация (LD, LC): | |
| LD50(средняя доза ) | нет данных |
| NIOSH (США пределы воздействия на здоровье): | |
| PEL (Допустимый) | [1 910.1027] TWA 0,005 мг / м (в виде Cd) |
| REL (рекомендуется) | Ca |
| IDLH (непосредственная опасность) | Ca [9 мг / м (в виде Cd)] |
| Кроме где указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на ink | |
Арсенид кадмия (Cd 3As 2) являются неорганический полуметалл семейства II-V. Он проявляет эффект Нернста.
Cd3As2диссоциирует между 220 и 280 ° C в соответствии с реакцией
Был обнаружен энергетический барьер для нестехиометрического испарения мышьяка из-за неравномерности парциальных давлений в зависимости от температуры. Диапазон запрещенной зоны составляет от 0,5 до 0,6 эВ. Cd 3As2плавится при 716 ° C и меняет фазу при 615 ° C /
Чистый арсенид кадмия претерпевает несколько фазовых переходов при высоких температурах, делая фазы, обозначенные α (стабильные), α ', α ”(метастабильный) и β. При 593 ° происходит полиморфный переход α → β.
Монокристаллическая дифракция рентгеновских лучей использовалась для определить параметры решетки Cd 3As2между 23 и 700 ° C. Переход α → α ′ происходит медленно и поэтому, скорее всего, является промежуточной фазой. Переход α ′ → α ″ происходит намного быстрее, чем α → α ′, и имеет очень небольшой тепловой гистерезис. Этот переход приводит к изменению оси четвертого порядка тетрагональной ячейки, вызывая двойникование кристалла . Ширина петли не зависит от скорости нагрева, хотя она становится уже после нескольких температурных циклов.
Соединение арсенида кадмия имеет более низкое давление пара (0,8 атм), чем оба кадмия. и мышьяк отдельно. Арсенид кадмия не разлагается при испарении и повторной конденсации. Концентрация носителей в Cd 3As2обычно составляет (1–4) × 10 электронов / см. Несмотря на высокую концентрацию носителей, подвижность электронов также очень высока (до 10 000 см / (В · с) при комнатной температуре).
В 2014 году было показано, что Cd 3As2является полуметаллом материал, аналогичный графену, который существует в трехмерной форме, который должно быть намного легче преобразовать в электронные устройства. Трехмерные (3D) топологические полуметаллы Дирака (TDS) являются объемными аналогами графена, которые также демонстрируют нетривиальную топологию в своей электронной структуре, которая имеет сходство с топологическими изоляторами. Более того, TDS потенциально может быть переведен в другие экзотические фазы (такие как полуметаллы Вейля, аксионные изоляторы и топологические сверхпроводники ), фотоэмиссионная спектроскопия с угловым разрешением выявила пару трехмерных Фермионы Дирака в Cd 3As2. По сравнению с другими трехмерными TDS, например, β-кристобалитом BiO. 2и Na3Bi, Cd 3As2стабилен и имеет гораздо более высокие скорости Ферми. Для настройки его энергии Ферми использовалось легирование на месте.
арсенид кадмия - это полупроводник II-V , демонстрирующий вырожденный полупроводник n-типа собственная проводимость с большой подвижностью, низкой эффективной массой и сильно непараболической зоной проводимости, или узкозонный полупроводник. Он отображает перевернутую зонную структуру, а оптическая энергетическая щель, e g, меньше 0. При осаждении термическим испарением (осаждением) арсенид кадмия имел вид Шоттки (термоэлектронная эмиссия ) и эффект Пула – Френкеля в сильных электрических полях.
Арсенид кадмия демонстрирует очень сильные квантовые осцилляции в стойкость даже при относительно высокой температуре 100К. Это делает его полезным для тестирования криомагнитных систем, так как наличие такого сильного сигнала является четким индикатором функции
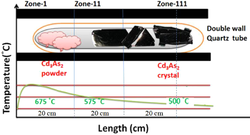 Схема роста кристаллов Cd 3As2из пара с использованием печи для оксида алюминия.
Схема роста кристаллов Cd 3As2из пара с использованием печи для оксида алюминия. Арсенид кадмия может быть получен в виде аморфного полупроводящего стекла. Согласно Хискоксу и Эллиоту, препарат арсенида кадмия производился из металлического кадмия, имеющего чистоту 6 N от компании Kock-Light Laboratories Limited. Хобокен поставил β-мышьяк чистотой 99,999%. Стехиометрические пропорции элементов кадмия и мышьяка были нагреты вместе. Разделение было трудным и длительным из-за того, что слитки прилипали к диоксиду кремния и ломались. Был создан жидкий инкапсулированный рост Stockbarger. Кристаллы извлекаются из летучих расплавов в жидкой капсуле. Расплав покрывается слоем инертной жидкости, обычно B 2O3, и применяется давление инертного газа, превышающее равновесное давление пара. Это исключает испарение расплава, что позволяет осуществлять затравку и вытягивание через слой B 2O3.
Элементарная ячейка Cd 3As2тетрагональная. Ионы мышьяка имеют плотную кубическую упаковку, а ионы кадмия координированы тетраэдрически. Пустые тетраэдрические участки спровоцировали исследования фон Штакельбергом и Паулюсом (1935), которые определили первичную структуру. Каждый ион мышьяка окружен ионами кадмия в шести из восьми углов искаженного куба, а два свободных места находились на диагоналях.
Кристаллическая структура арсенида кадмия очень похожа на структуру цинка. фосфид (Zn 3P2), арсенид цинка (Zn 3As2) и фосфид кадмия (Cd 3P2) ). Эти соединения четвертичной системы Zn-Cd-P-As представляют собой полностью непрерывный твердый раствор.
Арсенид кадмия используется в инфракрасных детекторах, использующих эффект Нернста, и в тонкопленочных динамических датчиках давления. также может использоваться для изготовления магниторезисторов, а в фотодетекторах.
арсенид кадмия может использоваться в качестве легирующей примеси для HgCdTe.
| Викискладе есть материалы, связанные с арсенидом кадмия. |