| аспарагинсинтетаза | |
|---|---|
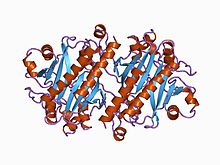 | |
| Идентификаторы | |
| Символ | ASNS |
| Альт. символы | 11as, AsnS |
| NCBI ген | 440 |
| HGNC | 753 |
| OMIM | 108370 |
| RefSeq | NM_001673 |
| UniProt | P08243 |
| Прочие данные | |
| Номер ЕС | 6.3.5.4 |
| Locus | Chr. 7 q21-q31 |
Аспарагинсинтетаза (или аспартат-аммиачная лигаза ) - это преимущественно цитоплазматический фермент, который генерирует аспарагин из аспартата. Эта реакция амидирования аналогична реакции, вызванной глутамин синтетазой. Фермент повсеместно распространен в органах млекопитающих, но базальная экспрессия относительно низка в тканях, кроме экзокринной поджелудочной железы.
Было связано присутствие аспарагинсинтетазы выше среднего в некоторых штаммах лейкемии быть значительным фактором устойчивости к химиотерапии, особенно к химиотерапевтическому препарату, L-аспарагиназа.
Аспарагинсинтетаза, полученная из Escherichia coli, представляет собой димерный белок, каждая субъединица которого сворачивается в два отдельных домена. N-концевая область состоит из двух слоев шестицепочечных антипараллельных β-листов, между которыми находится активный сайт, ответственный за гидролиз глутамина. С-концевой домен состоит из пятицепочечного параллельного β-слоя, фланкированного с обеих сторон α-спиралями. Этот домен отвечает за связывание как MgATP, так и аспартата. Эти два активных центра связаны туннелем, выстланным в основном атомами основной цепи и гидрофобными неполярными аминокислотными остатками.
Структурная характеристика аспарагинсинтетазы из источников млекопитающих была затруднена из-за низкой распространенности и нестабильности фермента во время процедуры очистки.
Используя информацию из аспарагинсинтетазы, полученной из Escherichia coli, были поняты некоторые основные механизмы действия фермента. N-концевой активный центр катализирует гидролиз глутамина с образованием глутамата и аммиака. C-концевой активный центр катализирует активацию карбоксилата боковой цепи аспартата с образованием электрофильного промежуточного соединения, β-аспартил-AMP (βAspAMP) 1 и неорганического пирофосфата (PPi ). Туннель, который связывает два активных центра, позволяет прохождению молекулы аммиака действовать как общий промежуточный продукт для связывания двух полуреакций, проводимых в независимых активных центрах фермента. Таким образом, после высвобождения в сайт глутаминазы и передачи из него молекула аммиака атакует связанный βAspAMP 1 с образованием аспарагина и AMP через тетраэдрическое промежуточное соединение.
В растениях неорганический азот поступает из окружающей среды в форме нитрата или аммония. Ассимиляция этого азота в аспарагин для использования в рециркуляции, транспортировке и хранении азота является важным процессом для развития растений, что делает аспарагинсинтетазу жизненно важной для поддержания этих запасов аспарагина. Конкретными событиями в развитии, которые зависят от аспарагинсинтетазы, являются мобилизация азота в прорастающих семенах, рециркуляция и поток азота в вегетативных клетках в ответ на биотические и абиотические стрессы и ремобилизация азота от источника к органам-поглотителям.
У млекопитающих аспарагин Было обнаружено, что экспрессия синтетазы связана с ростом клеток, а ее мРНК содержание связано с изменениями в клеточном цикле. Клетки ts11 хомяка BHK продуцируют неактивный фермент аспарагинсинтетазы, и эта потеря активности аспарагинсинтетазы непосредственно приводит к остановке клеточного цикла в клетках как следствие истощения клеточного аспарагина. В этих клетках хомяка также наблюдалась повышающая регуляция мРНК аспарагинсинтетазы. Другие эксперименты продемонстрировали, что покоящиеся клетки щитовидной железы крысы, входящие в фазу S в результате лечения тиреотропным гормоном, соответствовали одновременному увеличению содержания мРНК аспарагинсинтетазы.
По-видимому, существует две основные группы аспарагинсинтетазы:
Раковые клетки демонстрируют быстрый рост и деление клеток и, следовательно, имеют повышенную потребность в питании. Особенно низкий уровень экспрессии аспарагинсинтетазы при первичном остром лимфобластном лейкозе (ALL ) и многочисленных линиях клеток ALL по сравнению с нормальными клетками делает истощение запасов аспарагина эффективным методом лечение из-за необычной зависимости клеток от циркулирующего сывороточного аспарагина как необходимого питания для роста. В результате L-аспарагиназа является обычным химиотерапевтическим препаратом, используемым при лечении ОЛЛ, и может найти применение при других формах рака, отрицательных по аспарагинсинтетазе, таких как лимфомы, из-за своей активности аспаригиназы по истощению сывороточного аспарагина. Это истощение сывороточного аспарагина приводит к последующему быстрому оттоку клеточного аспарагина, который немедленно подвергается действию и разрушается также L-аспарагиназой. Из-за временной реакции этих восприимчивых раковых образований в ответ на истощение запасов аспарагина, рост опухоли значительно подавляется из-за дефицита питательных веществ.
Большинство соматических клеток экспрессируют достаточное базальное количество аспарагинсинтетазы, чтобы противодействовать этому голоданию аспарагина и выжить эффекты L-аспарагиназы. Кроме того, эти нормальные клетки способны повышать свою экспрессию аспарагинсинтетазы в ответ на истощение запасов аспарагина, дополнительно противодействуя некоторым токсическим эффектам лекарства на нормальную активность клеток, что является желательной чертой для химиотерапевтических препаратов.
Однако противоположный эффект наблюдается в случаях рака, устойчивого к аспарагиназе. При этих устойчивых раковых опухолях эффект истощения запасов аспарагина в крови за счет L-аспарагиназы вместо этого приводит к значительной избыточной экспрессии аспарагинсинтетазы для компенсации, эффективно сводя на нет эффект химиотерапевтического препарата. Например, в моделях мышей через 24 часа после воздействия L-аспарагиназы опухоли, устойчивые к истощению, реагировали 5-19-кратным увеличением экспрессии аспарагинсинтетазы. Эти устойчивые опухоли также по своей природе экспрессируют более высокие уровни активности аспарагинсинтетазы, даже без применения L-аспарагиназы для дальнейшей экспрессии. Подобные тенденции часто наблюдаются и в исследованиях на людях: высокие уровни активности аспарагинсинтетазы выявляются в случаях лечения, устойчивых к аспарагиназе, по сравнению с незначительной активностью в восприимчивых случаях. Как показали исследования in vitro устойчивых клеточных линий лейкемии человека, даже через шесть недель после удаления факторов, истощающих аспарагин, повышенный уровень экспрессии аспарагинсинтетазы не смог вернуться к исходному состоянию, вместо этого оставаясь повышенным и сохраняя постоянную устойчивость к лекарствам. 84>
Хотя механизмы, лежащие в основе устойчивой сверхэкспрессии ASNS, не были описаны в этих исследованиях, профилирование транскриптома двух пациентов с T-ALL, у которых возник рецидив после лечения L-аспарагиназой, выявило рецидивирующий обмен промотора с KMT2E, приводящий к ASNS. сверхэкспрессия и устойчивость к L-аспарагиназе. Кроме того, на модельных системах мышей было продемонстрировано, что повторное субкультивирование чувствительных к L-аспарагиназе опухолевых клеток в сублетальных концентрациях L-аспарагиназы может в конечном итоге сделать их устойчивыми, что может вызывать опасения по поводу лечения низкими дозами химиотерапии, эффективно стимулирующего развитие устойчивых клеток. 12>Возможный биомаркер рака яичников
Наблюдалась корреляция между эффективностью L-аспарагиназы и уровнями белка аспарагинсинтетазы в ряде линий клеток яичников человека. Как упоминалось выше, этот результат подтвердил аналогичные наблюдения на клеточных линиях лейкемии человека. Следовательно, аспарагинсинтетаза может быть использована в качестве биомаркера при скрининге рака яичников и потенциальном лечении.
Переход от эпителия к мезенхиме в метастатических клетках имитировался путем адаптации PC-3 Клетки рака предстательной железы из прикрепленных к суспензионной культуре, а затем исследованы для исследования изменений в экспрессии генов, одновременно с этой адаптацией к суспензии. Было обнаружено, что экспрессия аспарагинсинтетазы была в шесть раз выше в суспензионных клетках, чем в прикрепленных клетках. В ксенотрансплантатах из линии клеток рака молочной железы человека в установленной модели метастатических мышей уровень аспарагинсинтетазы был повышен в циркулирующих опухолевых клетках, выделенных из крови мышей, по сравнению с исходной линией клеток. Когда эти циркулирующие опухолевые клетки были возвращены в культуру in vitro и подверглись гипоксии, они показали более высокую базальную экспрессию и большую индукцию аспарагинсинтетазы, чем их родительская клеточная линия. Было также обнаружено, что эти циркулирующие опухолевые клетки обладают повышенной способностью к образованию колоний в анализах на мягком агаре в условиях гипоксии и росли быстрее при повторной имплантации в виде ксенотрансплантатов. Повышенная распространенность аспарагиназы синтетазы в метастатических клетках предполагает, что ее активность может быть полезной для выживания циркулирующих опухолевых клеток.
Морские свинки имеют одни из самых высоких уровней естественной экспрессии аспарагинсинтетазы из-за к тому факту, что их сыворотка изначально содержит определяемые уровни L-аспарагиназы.