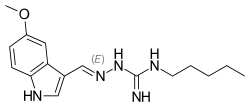 | |
 | |
| Клинические данные | |
|---|---|
| Торговые наименования | Zelnorm, Zelmac |
| AHFS / Drugs.com | Монография |
| Беременность. категория |
|
| Способы. введения | Пероральный |
| код ATC | |
| Правовой статус | |
| Правовой статус |
|
| Фармакокинетические данные | |
| Биодоступность | 10% |
| Связывание с белками | 98% |
| Метаболизм | Желудочный и печеночный |
| Период полувыведения | 11 ± 5 часов |
| Выведение | Кал и почек |
| Идентификаторы | |
Название ИЮПАК
| |
| Номер CAS | |
| PubChem CID | |
| IUPHAR / BPS | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| KEGG | |
| ChEMBL |
|
| CompTox Dashboard (EPA ) | |
| Химический a nd физические данные | |
| Формула | C16H23N5O |
| Молярная масса | 301,394 г · моль |
| 3D-модель (JSmol ) | |
УЛЫБКИ
| |
InChI
| |
| (что это?) | |
Тегасерод является 5-HT 4агонистом производства Novartis и продается под названиями Zelnorm и Zelmac для лечения синдрома раздраженного кишечника и запора. Одобренный FDA в 2002 году, он был впоследствии удален с рынка в 2007 году из-за опасений FDA по поводу возможных неблагоприятных сердечно-сосудистых эффектов. До этого это был единственный препарат, одобренный США Управлением по контролю за продуктами и лекарствами для облегчения дискомфорта в животе, вздутия живота, и запор, связанный с синдромом раздраженного кишечника. Его использование было также одобрено для лечения хронических идиопатических запоров.
Препарат действует как стимулятор моторики, достигая желаемого терапевтического эффекта. эффекты посредством активации 5-HT 4 рецепторов кишечной нервной системы в желудочно-кишечном тракте. Он также стимулирует моторику желудочно-кишечного тракта и перистальтический рефлекс и якобы уменьшает боль в животе. Кроме того, тегасерод является антагонистом рецептора 5-HT2B.
30 марта 2007 года в США Управление по санитарному надзору за качеством пищевых продуктов и медикаментов потребовало от компании Novartis снять тегасерод с полок. FDA заявило о взаимосвязи между назначением препарата и повышенным риском сердечного приступа или инсульта. Анализ данных, собранных на более чем 18 000 пациентов, продемонстрировал неблагоприятные сердечно-сосудистые события у 13 из 11 614 пациентов, получавших тегасерод (показатель 0,11%), по сравнению с 1 из 7 031 пациента, получавшего плацебо (показатель 0,01%). Компания Novartis утверждала, что у всех пораженных пациентов ранее были сердечно-сосудистые заболевания или факторы риска для них, а также утверждала, что причинно-следственная связь между использованием тегасерода и сердечно-сосудистыми событиями не была продемонстрирована. В тот же день, когда было объявлено FDA, Novartis Pharmaceuticals Canada объявила о приостановке маркетинга и продаж препарата в Канаде в ответ на запрос от Health Canada. В большом когортном исследовании, основанном на базе данных медицинского страхования США, при лечении тегасеродом не было обнаружено увеличения риска сердечно-сосудистых событий. В 2019 году тегасерод был повторно представлен для использования при синдроме раздраженного кишечника с запором (СРК-З) у женщин в возрасте до 65 лет.