| Перестановка Штиглица | |
|---|---|
| Названный в честь | Юлиус Штиглиц |
| Тип реакции | Реакция перестановки |
| Примеры и связанные реакции | |
| Подобные реакции | Перестановка Бекмана |
Перегруппировки Штиглица является реакция перегруппировки в органической химии, который назван в честь американского химика Юлий Штиглица (1867-1937) и впервые был исследован ним и Пол Николас Leech в 1913 г. Он описывает 1,2-перегруппировку из тритил аминных производных в триарильные имины. Это сравнимо с перегруппировкой Бекмана, которая также включает замещение атома азота через сдвиг углерода на азот. В качестве примера, триарильные гидроксиламины могут претерпевают перегруппировку Штиглицы путем дегидратацией и сдвиг в фенильную группе после активации с пентахлоридом фосфора с получением соответствующего триарильного имина, а основание Шифф.

В общем, термин «перегруппировка Штиглица» используется для описания широкого разнообразия реакций перегруппировки аминов в имины. Несмотря на то, что, как правило, связанно с перестройкой триарильных гидроксиламинов, которые хорошо изученными в научной литературе, Штиглицы перегруппировка может также происходить на алкилированных аминные производных, галоидаминах и азидах, а также другие активированных аминных производных.
 Механизм перегруппировки Бекмана
Механизм перегруппировки Бекмана Механизм реакции перегруппировки Штиглица, а также участвующие продукты и исходные материалы делают ее тесно связанной с перегруппировкой Бекмана, которая может быть использована для синтеза карбоксамидов. Обе реакции перегруппировки включают сдвиг углерода в азот, обычно после электрофильной активации уходящей группы на атоме азота. Однако основным отличием исходных материалов является их степень насыщения. В то время как перегруппировка Стиглица имеет место на насыщенных производных амина с одинарной σ-связью, типичным исходным материалом для перегруппировки Бекмана является оксим (гидроксилимин) с двойной связью C = N. В перегруппировках Бекмана, катализируемой кислота углерод миграции азота происходит на оксимо с образованием nitrilium иона промежуточного. В принципе, аналогично происходит и первый шаг перегруппировки Штиглица. Однако после генерации положительно заряженного иона имина через π-взаимодействие между неподеленной парой азота и электронодефицитным углеродом в перегруппировке Стиглица пути расходятся. В перегруппировке Штиглица нейтральное по заряду состояние молекулы может быть достигнуто путем диссоциации протона. Альтернативно, если исходный материал не содержал аминопротонов, нейтральное состояние может быть достигнуто с помощью внешнего восстанавливающего агента, такого как боргидрид натрия. Он восстанавливает промежуточное соединение иминиевый ион до соответствующего насыщенного амина. В перегруппировке Бекмана такой протон также отсутствует, и стабилизация промежуточного продукта происходит посредством нуклеофильного присоединения молекулы воды, диссоциации протона и таутомерии имидовой кислоты к карбоксамиду.
 Краткий, упрощенный и обобщенный механизм перегруппировки Стиглица, опосредованной кислотой Льюиса, Y = OH, OR, LA = кислота Льюиса = BF 3, «PCl 4 + »
Краткий, упрощенный и обобщенный механизм перегруппировки Стиглица, опосредованной кислотой Льюиса, Y = OH, OR, LA = кислота Льюиса = BF 3, «PCl 4 + » Хотя исходная реакция Стиглица наиболее известна перегруппировкой тритилгидроксиламинов, существует несколько вариантов, которые включают хорошие уходящие группы в качестве N -заместителей (таких как галогены и сульфонаты). Обычно применяются разные реагенты, в зависимости от конкретной природы субстрата.
Для перегруппировки тритилгидроксиламинов можно использовать кислоты Льюиса, такие как пентахлорид фосфора (PCl 5), пятиокись фосфора (P 2 O 5) или трифторид бора (BF 3). Они действуют как электрофильные активаторы гидроксильной группы, повышая качество уходящей группы. Например, при использовании PCl 5 в качестве реагента тритилгидроксиламин сначала превращается в активированный промежуточный продукт посредством нуклеофильного замещения. Образованный промежуточный продукт может затем подвергаться перегруппировке за счет миграции фенильной группы и диссоциации форм фосфора (V) с образованием N- фенилбензофенонамина.

Помимо N- гидрокситритиламинов, также возможны перегруппировки в N- алкокситритиламины. Однако эти реакции известны своим низким выходом. Например, N- бензилокси-замещенный тритиламин может подвергаться перегруппировке Стиглица в присутствии пентахлорида фосфора (160 ° C, выход 40%) или с BF 3 в качестве реагента (60 ° C, выход 29%). В последнем случае BF 3 действует как кислота Льюиса при электрофильной активации бензильного кислорода, чтобы сделать возможным нуклеофильную атаку на соседний атом азота.

Перегруппировки Штиглица также легко протекают с активными сульфонатами в качестве уходящей группы. N- сульфированные амины могут быть получены из соответствующих гидроксиламинов и подходящих реагентов сульфирования. Например, Herderin et al. синтезировали свой вторичный гидроксиламин (исходный материал в перегруппировке, показанной ниже), подвергая соответствующий гидроксиламин воздействию тозилхлорида и гидроксида натрия в ацетонитриле.
Перегруппировка Штиглица особенно реактивна в случае мостиковых бициклических N- сульфированных аминов в качестве исходных материалов, где мягкие условия являются достаточными для протекания эффективной реакции. Например, перегруппировка бициклического N- тозилированного амина легко протекает в водном диоксане при комнатной температуре. Однако соответствующий имин в этом случае не образуется, по-видимому, из-за напряжения, которое термодинамически не благоприятствовало бы такой структуре, несущей двойную связь у атома- мостика (правило Бредта ). Вместо этого тозилат добавляется нуклеофильно в геминальном положении азота посредством атаки на иминиевый ион.
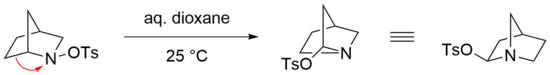
Перегруппировки Штиглица могут также протекать в органических азидах с молекулярным азотом в качестве хорошей уходящей группы. Эти реакции протекают аналогично стадиям реакции Шмидта, с помощью которых карбоновые кислоты могут быть преобразованы в амины путем добавления азойной кислоты в кислых водных условиях. Перегруппировка азидов Штиглица обычно выигрывает от протонной или термической активации, которые также можно комбинировать. В обоих случаях молекулярный азот высвобождается в виде газа необратимым образом. Было высказано предположение, что перегруппировка после диссоциации молекулы N 2 происходит через реакционноспособный промежуточный нитрен. Эти промежуточные продукты были бы очень похожи на те, которые были предложены в качестве ключевых промежуточных продуктов в реакциях перегруппировки, названных в честь Гофмана и Курциуса, но с тех пор считались маловероятными. При воздействии на азид кислоты Бренстеда протонирование азида активирует основной азот и снижает прочность связи с соседним, так что диссоциация и вытеснение молекулярного азота облегчаются. После перегруппировки протон может затем диссоциировать от иона иминия с образованием имина.
Альтернативным способом получения протонированных органических азидов является нуклеофильное присоединение гидразойной кислоты к карбокатионам, которые затем также могут претерпевать перегруппировки Стиглица.
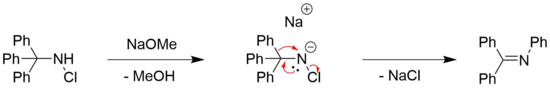
Перегруппировка Стиглица N- галогенированных аминов может наблюдаться для аминов, замещенных хлором и бромом, часто в сочетании с органическим основанием, таким как метоксид натрия. Потребность в основании обычно связана с необходимостью депротонирования амина.
Однако также сообщалось о примерах перегруппировок Штиглица без оснований N- галогенированных аминов. Пример этого можно найти в полном синтезе (±) -ликоподина Полом Грико и соавт. Здесь образование кольца происходит путем перегруппировки вторичного галогенамина, подвергая его тетрафторборату серебра. Известно, что AgBF 4 действует как источник ионов Ag +, который может способствовать диссоциации галогенидов от органических молекул с образованием соответствующего галогенида серебра в качестве движущей силы. Затем желаемый продукт получают восстановлением цианоборгидридом натрия, мягким восстанавливающим агентом, который обычно используется при восстановлении иминов до аминов.

Было также замечено, что добавление тетраацетата свинца может способствовать перегруппировке Штиглица производных амина. После образования активированного промежуточного соединения производного амина путем координации со свинцовым центром следующая перегруппировка снова протекает через миграцию ароматической группы с образованием связи C – N, диссоциацию свинца и депротонирование образующегося иона иминия.