 | |
 | |
 | |
| Имена | |
|---|---|
| Другие названия Пероксодисульфат натрия. Пероксодисульфат натрия. Пероксидисульфат натрия. Пероксидисульфат натрия | |
| Идентификаторы | |
| Номер CAS | |
| 3D-модель (JSmol ) | |
| ChEMBL |
|
| ChemSpider | |
| ECHA InfoCard | 100.028.993 |
| Номер EC |
|
| PubChem CID | |
| номер RTECS |
|
| UNII | |
| номер ООН | 1505 |
| CompTox Dashboard (EPA ) | |
InChI
| |
УЛЫБКА
| |
| Свойства | |
| Химическая формула | Na2S2O8 |
| Молярная масса | 238,10 г / моль |
| Внешний вид | белый порошок |
| Плотность | 2,59 г / см. (насыпная плотность в насыпном состоянии: 1,12 г / см) |
| Температура плавления | 180 ° C (356 ° F; 453 K) разлагается |
| Растворимость в воде | 55,6 г / 100 мл (20 ° C) |
| Опасности | |
| Паспорт безопасности | ICSC 1136 |
| Пиктограммы GHS |    |
| Сигнальное слово GHS | Опасно |
| Краткая характеристика опасности GHS | H272, H302, H315, H317, H319, H334, H335, H371 |
| Меры предосторожности GHS | P220, P261, P280, P305 + 351 + 338, P342 + 311 |
| NFPA 704 (огненный алмаз) |  0 2 1 OX 0 2 1 OX |
| Температура вспышки | Невоспламеняющийся |
| Родственные соединения | |
| Прочие анионы | Дитионит натрия. Сульфит натрия. Сульфат натрия |
| Прочие катионы | Персульфат калия |
| Если не указано иное, данные для материалов приведены в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки в ink | |
Персульфат натрия представляет собой неорганическое соединение формулы Na 2S2 O8. Это натриевая соль пероксидисерной кислоты, H 2S2O8, окислитель. Это белое твердое вещество, растворяющееся в воде. Он почти не гигроскопичен и имеет хороший срок хранения.
Соль приготовлена путем электролитического окисления гидросульфата натрия :
Окисление проводят на платиновом аноде. Таким образом в 2005 году было произведено около 165 000 тонн.
Стандартный окислительно-восстановительный потенциал персульфата натрия в гидросульфат составляет 2,1 В, что выше, чем у пероксида водорода (1,8 В), но ниже, чем у озона (2,2 В.). Сульфатный радикал, образующийся in situ, имеет стандартный электродный потенциал 2,7 В.
Однако есть несколько недостатков в использовании платиновых анодов для получения солей; производственный процесс неэффективен из-за выделения кислорода, и продукт может содержать загрязняющие вещества, возникающие в результате коррозии платины (в основном из-за чрезвычайно окислительной природы сульфатного радикала). Таким образом, алмазные электроды, легированные бором, были предложены в качестве альтернативы обычным платиновым электродам.
В основном он используется в качестве радикального инициатора для эмульсии. реакции полимеризации для полимеров на основе стирола, таких как акрилонитрилбутадиенстирол. Также применимо для ускоренного отверждения клеев с низким содержанием формальдегида.
Это отбеливатель, как автономный (особенно в косметике для волос), так и в качестве моющего компонента. Он заменяет персульфат аммония в травильных смесях для цинка и печатных плат и используется для травления из меди и некоторых других металлов.
Он также используется в качестве кондиционера почвы и для восстановления почвы и грунтовых вод, а также при производстве красителей, модификации крахмала., активатор отбеливания, дезинфицирующий агент для окислительной дезинфекции и т. Д.
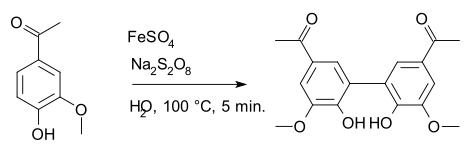
Персульфат натрия - специализированный окислитель агент в химии, обычно в реакциях окисления персульфата Эльбса и реакции окисления Бойленда – Симса. Он также используется в радикальных реакциях; например, при синтезе диапоцинина из апоцинина, где сульфат железа (II) является радикальным инициатором.
Соль является окислителем и образует горючие смеси с такими органическими материалами, как бумага. Сильные восстановители, такие как магний, при смешивании могут образовывать взрывоопасные композиции.