 Неправильно свернутые белки могут образовывать белковые агрегаты или амилоидные фибриллы, разрушаться или возвращаться к своей естественной структуре.
Неправильно свернутые белки могут образовывать белковые агрегаты или амилоидные фибриллы, разрушаться или возвращаться к своей естественной структуре. Агрегация белков представляет собой биологический феномен, при котором внутренне неупорядоченные белки или неправильно свернутые белки агрегируются (т.е. накапливаются и слипаются) внутри- или внеклеточно. Неправильно свернутые белковые агрегаты часто коррелируют с заболеваниями. Фактически, белковые агрегаты участвуют в большом количестве заболеваний, известных как амилоидозы, включая ALS, болезнь Альцгеймера, болезнь Паркинсона и прионная болезнь.
После синтеза белки обычно складываются в конкретную трехмерную конформацию, которая является наиболее термодинамически благоприятной: их нативное состояние. Этот процесс сворачивания обусловлен гидрофобным эффектом : склонностью гидрофобных (водобоязненных) частей белка защищаться от гидрофильной (водолюбивой) среды клетки, погружаясь во внутреннюю часть клетки. белок. Таким образом, внешняя часть белка обычно гидрофильна, тогда как внутренняя часть обычно гидрофобна.
Белковые структуры стабилизируются нековалентными взаимодействиями и дисульфидными связями между двумя остатками цистеина. Нековалентные взаимодействия включают ионные взаимодействия и слабые ван-дер-ваальсовы взаимодействия. Ионные взаимодействия образуются между анионом и катионом и образуют солевые мостики, которые помогают стабилизировать белок. Ван-дер-ваальсовы взаимодействия включают неполярные взаимодействия (т.е. лондонская дисперсионная сила ) и полярные взаимодействия (т.е. водородные связи, диполь-дипольные связи ). Они играют важную роль во вторичной структуре белка, такой как формирование альфа-спирали или бета-листа, и третичной структуре. Взаимодействия между аминокислотными остатками в конкретном белке очень важны для окончательной структуры этого белка.
Когда происходят изменения в нековалентных взаимодействиях, что может произойти при изменении аминокислотной последовательности, белок подвержен неправильной укладке или разворачиванию. В этих случаях, если клетка не способствует повторной сворачиванию белка или не разрушает развернутый белок, развернутый / неправильно свернутый белок может агрегироваться, в результате чего открытые гидрофобные части белка могут взаимодействовать с открытыми гидрофобными участками других белков.. Существует три основных типа белковых агрегатов, которые могут образовываться: аморфные агрегаты, олигомеры и амилоидные фибриллы.
Агрегация белка может происходить по разным причинам. Эти причины можно разделить на четыре класса, которые подробно описаны ниже.
Мутации, которые происходят в последовательности ДНК, могут влиять или не влиять на аминокислотную последовательность белка. Когда последовательность затронута, другая аминокислота может изменить взаимодействия между боковыми цепями, которые влияют на укладку белка. Это может привести к появлению открытых гидрофобных областей белка, которые агрегируются с тем же неправильно свернутым / развернутым белком или с другим белком.
Помимо мутаций в самих затронутых белках, агрегация белков также может быть вызвана косвенно через мутации белков в регуляторных путях, таких как путь рефолдинга (молекулярные шапероны ) или Путь убиквитин-протеасома (убиквитинлигазы). Шапероны помогают в рефолдинге белка, обеспечивая безопасную среду для сворачивания белка. Убиквитин лигазирует целевые белки для деградации посредством модификации убиквитина.
Агрегация белка может быть вызвана проблемами, возникающими во время транскрипции или трансляции. Во время транскрипции ДНК копируется в мРНК, образуя цепь пре-мРНК, которая подвергается процессингу РНК с образованием мРНК. Во время трансляции рибосомы и тРНК помогают транслировать последовательность мРНК в аминокислотную последовательность. Если на любом этапе возникают проблемы, связанные с получением неправильной цепи мРНК и / или неправильной аминокислотной последовательности, это может вызвать неправильную укладку белка, что приведет к агрегации белка.
Экологические стрессы, такие как экстремальные температуры и pH или окислительный стресс, также могут привести к агрегации белков. Одним из таких заболеваний является криоглобулинемия.
Экстремальные температуры могут ослаблять и дестабилизировать нековалентные взаимодействия между аминокислотными остатками. Значения pH за пределами диапазона pH белка могут изменить состояние протонирования аминокислот, что может увеличить или уменьшить нековалентные взаимодействия. Это также может привести к менее стабильным взаимодействиям и к разворачиванию белков.
Окислительный стресс может быть вызван такими радикалами, как активные формы кислорода (ROS). Эти нестабильные радикалы могут атаковать аминокислотные остатки, приводя к окислению боковых цепей (например, ароматических боковых цепей, метионин боковых цепей) и / или разрыву полипептидных связей. Это может повлиять на нековалентные взаимодействия, которые правильно удерживают белок вместе, что может вызвать дестабилизацию белка и может вызвать его разворачивание.
Клетки имеют механизмы, которые могут повторно складываться или разрушаться белковые агрегаты. Однако по мере старения клетки эти механизмы контроля ослабевают, и клетка становится менее способной разделять агрегаты.
Гипотеза о том, что агрегация белков является причинным процессом старения, теперь проверена, поскольку некоторые модели замедленного старения находятся в стадии разработки. рука. Если развитие белковых агрегатов было процессом, не зависящим от старения, замедление старения не повлияет на скорость протеотоксичности с течением времени. Однако если старение связано со снижением активности защитных механизмов против протеотоксичности, модели медленного старения покажут снижение агрегации и протеотоксичности. Для решения этой проблемы было проведено несколько анализов токсичности C. elegans. Эти исследования показали, что снижение активности передачи сигналов инсулина / IGF (IIS), важного пути регуляции старения, защищает от связанной с нейродегенерацией агрегации токсичных белков. Обоснованность этого подхода была проверена и подтверждена на млекопитающих, поскольку снижение активности сигнального пути IGF-1 защищает мышей с моделью болезни Альцгеймера от поведенческих и биохимических нарушений, связанных с этим заболеванием.
Несколько исследований показали, что клеточные ответы на агрегацию белков хорошо регулируются и организованы. Белковые агрегаты локализуются в определенных областях клетки, и были проведены исследования этих локализаций у прокариот (кишечная палочка) и эукариот (дрожжи, клетки млекопитающих).
Агрегаты в бактериях асимметрично заканчиваются на одном из полюсов клетки, «старом полюсе». После деления клетки дочерние клетки со старшим полюсом получают белковый агрегат и растут медленнее, чем дочерние клетки без агрегата. Это обеспечивает механизм естественного отбора для уменьшения белковых агрегатов в бактериальной популяции.
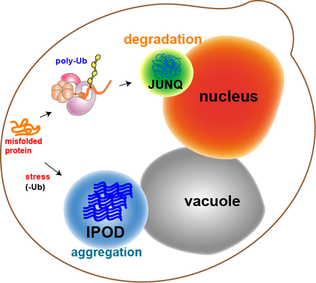
Большинство белковых агрегатов в дрожжевых клетках подвергаются повторной укладке с помощью молекулярных шаперонов. Однако некоторые агрегаты, такие как окислительно поврежденные белки или белки, предназначенные для деградации, не могут быть повторно свернуты. Скорее, есть два отсека, в которые они могут попасть. Белковые агрегаты могут быть локализованы в юкстаноуклеарном отсеке контроля качества (JUNQ ), который находится рядом с ядерной мембраной, или в отложении нерастворимого белка (IPOD ), рядом с вакуолью в дрожжевых клетках. Белковые агрегаты локализуются в JUNQ, когда они убиквитинируются и нацелены на деградацию. Агрегированные и нерастворимые белки локализуются на IPOD в виде более постоянного отложения. Есть свидетельства того, что белки здесь могут быть удалены путем аутофагии. Эти два пути работают вместе в том смысле, что белки имеют тенденцию поступать в IPOD, когда протеасомный путь перегружается.
В клетках млекопитающих эти белковые агрегаты называют «агресомами» и они образуются при заболевании клетки. Это связано с тем, что агрегаты имеют тенденцию к образованию, когда в клетке присутствуют гетерологичные белки, что может возникнуть при мутации клетки. Убиквитинлигаза E3 способна распознавать неправильно свернутые белки и убихинировать их. HDAC6 может затем связываться с убиквитином и моторным белком динеином, чтобы доставить меченые агрегаты в центр организации микротрубочек (MTOC ). Там они собираются вместе в сферу, окружающую MTOC. Они переносят шапероны и протеасомы и активируют аутофагию.
В клетке есть две основные системы контроля качества белка, которые отвечают за устранение агрегатов белка. Неправильно уложенные белки могут подвергаться повторной укладке с помощью бишапероновой системы или разрушаться системой убиквитиновых протеасом или аутофагией.
Бишапероновая система использует Hsp70 (DnaK-DnaJ-GrpE в E.coli и Ssa1-Ydj1 / Sis1-Sse1 / Fe1 в дрожжах) и Hsp100 (ClpB в E. coli и Hsp104 в дрожжах) шапероны для дезагрегации и рефолдинга белков.
Hsp70 взаимодействует с белковыми агрегатами и рекрутирует Hsp100. Hsp70 стабилизирует активированный Hsp100. Белки Hsp100 имеют ароматические петли пор, которые используются для распутывания отдельных полипептидов. Эта нитевидная активность может быть инициирована на N-конце, C-конце или в середине полипептида. Полипептид транслоцируется через Hsp100 в несколько этапов, используя АТФ на каждом этапе. Полипептид разворачивается, а затем ему дают возможность свернуться либо самостоятельно, либо с помощью белков теплового шока.
Неправильно свернутые белки могут быть устранены через систему убиквитин-протеасома (UPS ). Он состоит из пути E1-E2-E3, который убихинирует белки, чтобы пометить их для деградации. У эукариот белки расщепляются протеасомой 26S. В клетках млекопитающих лигаза E3, карбоксиконцевой белок, взаимодействующий с Hsp70 (CHIP), нацелен на белки, связанные с Hsp70. В дрожжах лигазы E3 Doa10 и Hrd1 имеют сходные функции в отношении белков эндоплазматического ретикулума.

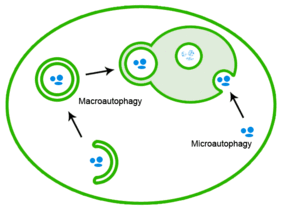
Неправильно свернутые белки также могут быть устранены посредством аутофагии, при которой агрегаты белка доставляются в лизосомы.
Хотя считалось, что зрелые белковые агрегаты токсичны, недавние данные свидетельствуют о том, что на самом деле наиболее токсичными являются незрелые белковые агрегаты. Гидрофобные участки этих агрегатов могут взаимодействовать с другими компонентами клетки и повреждать их. Гипотезы состоят в том, что токсичность белковых агрегатов связана с механизмами секвестрации клеточных компонентов, генерации активных форм кислорода и связывания со специфическими рецепторами в мембране или через разрушение мембран. Количественный анализ был использован для определения того, что частицы с более высокой молекулярной массой ответственны за проникновение через мембрану. Известно, что белковые агрегаты in vitro могут дестабилизировать искусственные бислои фосфолипидов, приводя к пермеабилизации мембраны.