 | |
| Имена | |
|---|---|
| Название ИЮПАК оксалат магния | |
| Систематическое название ИЮПАК оксалат магния | |
| Другие имена | |
| Идентификаторы | |
| Количество CAS | |
| 3D модель ( JSmol ) | |
| ChemSpider | |
| ECHA InfoCard | 100.008.121 |
| Номер ЕС | |
| PubChem CID | |
| UNII | |
| Номер ООН | 2811 |
| Панель управления CompTox ( EPA) | |
ИнЧИ
| |
Улыбки
| |
| Характеристики | |
| Химическая формула | |
| Молярная масса | |
| Появление | белое твердое вещество |
| Плотность | 2,45 г / см 3 |
| Температура плавления | от 420 до 620 ° C (от 788 до 1148 ° F; от 693 до 893 K) до 150 ° C (302 ° F, 423 K) (дигидрат) оба разлагаются |
| Точка кипения | Непригодный |
| Растворимость в воде | 0,038 г / 100 г H 2 O (безводной и дигидратной) |
| Произведение растворимости ( K уд) | 8,5 × 10-5 для MgC 2О 4 |
| Растворимость | не растворим в органических веществах |
| Давление газа | 2,51 × 10 -6 мм рт.ст. |
| Термохимия | |
| Std энтальпия формации (Δ F H ⦵298) | -1269.0 кДж моль -1 |
| Опасности | |
| Основные опасности | Раздражающий |
| NFPA 704 (огненный алмаз) |  1 0 0 1 0 0 |
| точка возгорания | Непригодный |
| самовоспламенения температуру | Непригодный |
| Родственные соединения | |
| Родственные соединения | Оксид магния |
| Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
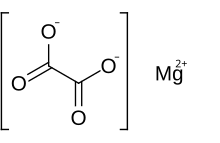
Оксалат магния - это органическое соединение, содержащее катион магния с зарядом 2+, связанный с оксалат- анионом. Он имеет химическую формулу MgC 2 O 4. Оксалат магния представляет собой белое твердое вещество, которое бывает двух форм: безводной и дигидратной, где две молекулы воды образуют комплекс со структурой. Обе формы практически не растворимы в воде и нерастворимы в органических растворах.
Оксалат магния был обнаружен в естественных условиях около завода в Джонстон, который расположен недалеко от Инша на северо-востоке Шотландии. Этот природный оксалат магния называется глушинскитом и встречается на границе раздела лишайник / порода на серпентините в виде кремово-белого слоя, смешанного с гифами лишайникового гриба. Сканирующие электронный микроскоп образцов, взятый показал, что кристаллы имели пирамидальную структуру с обеими изогнутых и полосатыми гранями. Размер этих кристаллов составлял от 2 до 5 мкм.
Оксалат магния можно синтезировать путем объединения соли или иона магния с оксалатом.
Конкретным примером синтеза может быть смешивание Mg (NO 3) 2 и KOH с последующим добавлением этого раствора к диметилоксалату (COOCH 3) 2.
При нагревании оксалат магния разлагается. Во-первых, дигидрат разлагается при 150 ° C до безводной формы.
При дополнительном нагревании безводная форма будет далее разлагаться на оксид магния и оксиды углерода при температуре от 420 ° C до 620 ° C. Сначала образуются окись углерода и карбонат магния. Затем монооксид углерода окисляется до диоксида углерода, а карбонат магния далее разлагается до оксида магния и диоксида углерода.
Дигидрат оксалата магния также использовался в синтезе наноразмерных частиц оксида магния, которые имеют большее отношение поверхности к объему, чем частицы, синтезированные обычным способом, и оптимальны для различных применений, таких как катализ. Используя золь-гель синтез, который включает объединение соли магния, в данном случае оксалата магния, с желатинирующим агентом, можно получить наноразмерные частицы оксида магния.
Оксалат магния раздражает кожу и глаза. При вдыхании вызывает раздражение легких и слизистых оболочек. Оксалат магния не имеет известных хронических или канцерогенных эффектов. Оксалат магния негорюч и стабилен, но в условиях пожара выделяет токсичные пары. Согласно OSHA, оксалат магния считается опасным.