| |||
 | |||
| Имена | |||
|---|---|---|---|
| Другие имена Трихлорид гадолиния | |||
| Идентификаторы | |||
| Номер CAS |
| ||
| 3D-модель (JSmol ) | |||
| ChEBI | |||
| ChEMBL |
| ||
| ChemSpider | |||
| ECHA InfoCard | 100.030.338 | ||
| PubChem CID | |||
| UNII | |||
| Панель управления CompTox (EPA ) | |||
InChI
| |||
УЛЫБКИ
| |||
| Свойства | |||
| Химическая формула | GdCl 3 | ||
| Молярная масса | 263,61 г / моль | ||
| Внешний вид | белые кристаллы. гигроскопичен | ||
| Плотность | 4,52 г / см | ||
| Точка плавления | 609 ° C (1128 ° F; 882 K) | ||
| Температура кипения | 1580 ° C (2880 ° F, 1850 K) | ||
| Растворимость в воде | 94,65 г / 100 мл, 25 ° C | ||
| Магнитная восприимчивость (χ) | + 27,930 · 10 см / моль | ||
| Структура | |||
| Кристаллическая структура | гексагональная, hP8 | ||
| Пространственная группа | P63/ м, № 176 | ||
| Родственные соединения | |||
| Другие анионы | Оксид гадолиния (III) | ||
| Другие катионы | Европий (III) хлорид, хлорид тербия (III) | ||
| Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |||
| Ссылки в ink | |||
Хлорид гадолиния (III), также известный как трихлорид гадолиния, представляет собой GdCl 3. Это бесцветное гигроскопичное водорастворимое твердое вещество. гексагидрат GdCl 3 ∙ 6H 2 O обычно встречается и иногда также называется трихлоридом гадолиния. Виды Gd представляют особый интерес, потому что ион имеет максимально возможное число неспаренных спинов, по крайней мере, для известных элементов. Имея семь валентных электронов и семь доступных f-орбиталей, все семь электронов неспарены и симметрично расположены вокруг металла. Сочетание высокого магнетизма и высокой симметрии делает Gd полезным компонентом в спектроскопии ЯМР и МРТ.
GdCl 3 обычно готовится способом «хлорид аммония », который включает начальный синтез (NH 4)2[GdCl 5 ]. Этот материал может быть получен из обычных исходных материалов при температурах реакции 230 ° C из оксида гадолиния :
из гидратированного хлорида гадолиния:
из металла гадолиний :
На второй стадии пентахлорид разлагается при 300 ° C:
Эта реакция пиролиза протекает через промежуточное соединение NH 4 [Gd 2Cl7].
Метод хлорида аммония более популярен и сс дороже, чем другие методы. Однако GdCl 3 также может быть синтезирован реакцией твердого Gd при 600 ° C в проточном потоке HCl.
Хлорид гадолиния (III) также образует гексагидрат, GdCl 3 ∙ 6H 2 O. Гексагидрат получают из оксида (или хлорида) гадолиния (III) в концентрированной HCl с последующим выпариванием.
GdCl 3 кристаллизуется с гексагональная структура UCl 3, как видно для других 4f трихлоридов, включая таковые La, Ce, Pr, Nd, Pm, Sm, Eu. В мотиве YCl 3 кристаллизуются следующие вещества: DyCl 3, HoCl 3, ErCl 3, TmCl 3, YdCl 3, LuCl 3, YCl 3). Мотив UCl 3 представляет собой 9-координатный металл с треугольной призматической треугольной зоной координационной сферой. В гексагидрате хлорида гадолиния (III) и других более мелких 4f трихлоридах и трибромидах шесть молекул H 2O и 2 иона Cl координируются с катионами, что приводит к координации группа из 8.
Соли гадолиния представляют основной интерес для агентов релаксации в магнитно-резонансной томографии (МРТ ). Этот метод использует тот факт, что Gd имеет электронную конфигурацию f. Семь - это самое большое количество неспаренных электронных спинов, возможное для атома, поэтому Gd является ключевым компонентом при создании высокопарамагнитных комплексов. Для создания релаксационных агентов источники Gd, такие как GdCl 3 ∙ 6H 2 O, превращаются в координационные комплексы. GdCl 3 ∙ 6H 2 O не может использоваться в качестве контрастирующего агента MRI из-за его низкой растворимости в воде при почти нейтральном pH организма. «Свободный» гадолиний (III), например [GdCl 2(H2O)6] токсичен, поэтому хелатирующие агенты необходимы для биомедицинских применений. Простых монодентатных или даже бидентатных лигандов недостаточно, потому что они не остаются связанными с Gd в растворе. Следовательно, требуются лиганды с более высокими координационными числами. Очевидным кандидатом является ЭДТА, этилендиаминтетраацетат, который представляет собой обычно используемый гексадентатный лиганд, используемый для образования комплексов с переходными металлами. Однако в лантаноидах координационные числа больше шести, поэтому используются еще более крупные аминокарбоксилаты.
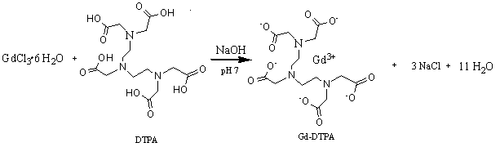
Одним типичным хелатирующим агентом является H 5 DTPA, диэтилентриаминпентауксусная кислота. Хелатирование с основанием конъюгата этого лиганда увеличивает растворимость Gd при нейтральном pH организма и по-прежнему допускает парамагнитный эффект, необходимый для МРТ контрастного агента.. Лиганд DTPA связывается с Gd через пять атомов кислорода карбоксилатов и три атома азота аминов. Остается 9-й сайт связывания, который занимает молекула воды. Быстрый обмен этого водного лиганда с объемной водой является основной причиной свойств хелата по усилению сигнала. Структура [Gd (DTPA) (H 2 O)] представляет собой искаженную треугольную призму с тремя углами.
Ниже приводится реакция образования Gd-DTPA: