Археол - один из основных липидов мембран архей, одной из трех областей жизни. Одна из ключевых особенностей, которая отличает архей от бактерий и эукарион, - это их мембранные липиды, в которых археол играет важную роль. Из-за этого археол также широко используется в качестве биомаркера активности древних архей, особенно метаногенов.
Археол обычно состоит из соединения двух фитанильных цепей с sn-2 и sn- 3 положения молекулы глицерина. Предполагается, что сильно разветвленные боковые цепи объясняют очень низкую проницаемость мембраны на основе археол, которая может быть одной из ключевых адаптаций архей к экстремальным условиям окружающей среды.
 | |
| Имена | |
|---|---|
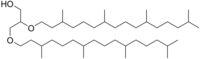
| Название ИЮПАК 2,3-Бис (3,7,11,15-тетраметилгексадекокси) пропан-1-ол | |
| Другие названия Липид археол ; 2,3-ди-O-фитанил-sn-глицерин; 2,3-Бис [(3,7,11,15-тетраметилгексадецил) окси] -1-пропанол | |
| Идентификаторы | |
| Номер CAS | |
| 3D-модель (JSmol ) | |
| MeSH | археол + липид |
| PubChem CID | |
| CompTox Dashboard (EPA ) | |
УЛЫБКИ
| |
| Свойства | |
| Химическая формула | C43H88O3 |
| Молярная масса | 653,174 г · моль |
| Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобокс | |
Археол - диэфирный липид, обычно встречающийся в Стандартные археолы представляют собой 2,3-ди-O-фитанил-sn- глицерин, с двумя фитанильными цепями, связывающимися с положение sn-2 и sn-3 глицерина по эфирным связям. Структура 2,3-sn-глицерина и связь простых эфиров являются двумя ключевыми отличиями липидов архей от липидов бактерий и эукариот, которые используют 1,2-sn-глицерин, и в основном, сложноэфирные связи. Природный археол имеет конфигурации 3R, 7R, 11R для трех хиральных центров в изопреноидных цепях. Существует четыре структурных вариации, которые усложняют мембранные липиды по функциям и свойствам. Две фитанильные цепи могут образовывать 36-членное кольцо, давая макроциклический археол. Гидроксилированный археол имеет фитанильные цепи, гидроксилированные по первому третичному атому углерода, тогда как сестертерпаниловый археол имеет фитанильные боковые цепи с C25-сестертерерпанильными цепями, замещающими у C2 глицерина или по обоим атомам углерода. Ненасыщенный археол с тем же углеродным скелетом, что и стандартный археол, но также обнаружен одна или несколько двойных связей в боковых цепях фитанила.
Две молекулы археола могут подвергаться прямому соединению с образованием кальдархеола (один типичный тетраэфир диалкилглицерина глицерина, GDGT), один из наиболее распространенных тетраэфирных липидов у архей.
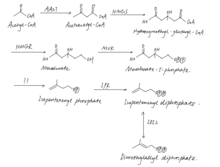 Альтернативный путь MVA, занятый в клетках архей для синтеза изопреноидных цепей архей. Последние три стадии (катализируемые неизвестным ферментом ??, IPK и IDI2, соответственно) отличаются от типичного пути MVA.
Альтернативный путь MVA, занятый в клетках архей для синтеза изопреноидных цепей архей. Последние три стадии (катализируемые неизвестным ферментом ??, IPK и IDI2, соответственно) отличаются от типичного пути MVA. 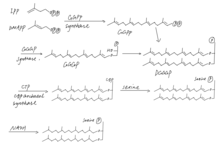 Синтез фосфолипидов на основе архей в архее. Изопреноидные боковые цепи происходят из IPP и DMAPP, которые синтезируются с помощью альтернативных путей MVA.
Синтез фосфолипидов на основе архей в архее. Изопреноидные боковые цепи происходят из IPP и DMAPP, которые синтезируются с помощью альтернативных путей MVA.  Стандартный археол, образованный путем связывания двух фитанильных цепей с sn-2 и sn-3 положениями молекулы глицерина.
Стандартный археол, образованный путем связывания двух фитанильных цепей с sn-2 и sn-3 положениями молекулы глицерина.  Макроциклический археол, образованный путем соединения концов двух фитанильных цепей в стандартном археоле.
Макроциклический археол, образованный путем соединения концов двух фитанильных цепей в стандартном археоле.  Гидроксильный археол с гидроксилированной фитанильной цепью по первому третичному атому углерода.
Гидроксильный археол с гидроксилированной фитанильной цепью по первому третичному атому углерода.  Сестертерпаниловый археол, образованный замещением фитаниловых (С20) цепей в стандартный археол цепями сестертерпанила (C25).
Сестертерпаниловый археол, образованный замещением фитаниловых (С20) цепей в стандартный археол цепями сестертерпанила (C25).  Ненасыщенный археол, образованный введением двойных связей в стандартный археол.
Ненасыщенный археол, образованный введением двойных связей в стандартный археол. Обнаружен археол во всех проанализированных архей, по крайней мере, следовое количество. Он составляет 100% липидов диэфирного ядра в большинстве нейтрофилов галофилов и серозависимых термофилов (хотя их основные липиды ядра являются тетраэфирными липидами). Метаногены содержат гидроксиархеол и макроциклические соединения, отличные от стандартных археол, а археол, содержащий сестертерпаниловую цепь, характерен для алкалифильных крайних галофилов. Примечательно, что тетраэфирные липиды также широко присутствуют в архее.
Липосомы (сферическая везикула, имеющая по крайней мере один липидный бислой) липидов из архей обычно демонстрируют чрезвычайно низкую проницаемость для молекул и ионы, включая протоны. Ионная проницаемость, индуцированная ионофорами (переносчиками ионов через мембраны), также довольно низкая и сопоставима только с проницаемостью яичного фосфатидилхолина (очень распространенный компонент биологических мембран) при 37 ° C. когда температура поднимается до ок. 70˚C. По сравнению с бактериями и эукариотами, изопреноидные боковые цепи археола сильно разветвлены. Считается, что это структурное различие снижает проницаемость архей во всем диапазоне температур роста, что позволяет археям адаптироваться к экстремальным условиям окружающей среды.
Археолы обычно обнаруживаются в виде фосфолипидов в клетках архей. Синтетический путь полностью насыщенного археолфосфолипида протекает следующим образом: синтез изопреноидных боковых цепей за счет соединения изопренов голова-хвост, эфирная связь с глицерин-1-фосфатным остовом, образование археол ЦДФ, присоединение полярной головной группы и насыщение двойной облигации. После этого, тетраэфирные липиды могут быть синтезированы впоследствии реакцией димеризации через связь голова к голове.
Археи обладают разными путями биосинтеза изопреноидных цепей по сравнению с бактериями и эукариями. Предшественниками изопреноида являются звенья C5 изопентенилпирофосфат (IPP) и диметилаллилпирофосфат (DMAPP), которые универсальны для всех трех сфер жизни. Как правило, два соединения синтезируются в бактериях через 2-C-метил-D-эритритол 4-фосфат / 1-дезокси-D-ксилулозо-5-фосфатный путь (путь MEP / DOXP) и синтезируются через путь мевалоната (MVA). в большинстве эукарий. Синтез IPP и DMAPP в архее происходит по альтернативному пути MVA, который отличается от классического пути MVA на последних трех этапах и разделяет остальные четыре этапа.
Хотя археол, показывающий эфирную связь между изопреноидной цепью и глицерином, считается убедительным биомаркером для архей, липиды эфирных мембран также были обнаружены у некоторых аэробных и анаэробных бактерий, включая липиды с одна сложноэфирная связь и одна эфирная связь с алкильными цепями. Многие строго аноксические бактерии и несколько аэробных видов содержат плазмалогены (Pla), у которых есть алкильная цепь, связанная с sn-1 положением глицерина посредством винилэфирной связи. Считается, что, как и археи, эти липиды увеличивают устойчивость бактерий к неблагоприятным условиям окружающей среды. Еще более поразительным является открытие неизопреноидных диэфирных липидов диалкилглицерина (DGD) и разветвленных диалкилглицериновых тетраэфирных липидов (brGDGT), которые образуются аналогично археолу путем связывания алкильных цепей (но не изопреноидных цепей) с молекулами глицерина через эфир. связь. Примечательно, что эти липиды отличаются от липидов эфиров архей только боковыми цепями и позициями связывания на глицерине. Сообщается о DGD у термофильных бактерий, некоторых мезофильных бактерий и агрегирующих миксобактерий.
Археол в отложениях обычно возникает в результате гидролиза фосфолипидов мембран архей. во время диагенеза. Из-за его высокого потенциала сохранения он часто обнаруживается и используется геохимиками-органиками в качестве биомаркера активности архей, особенно биомассы и активности метаногена. В качестве заместителя метаногена он используется Michinari Sunamura et al. для прямого измерения метаногенов в отложениях Токийского залива, а также использовался Кэти Л. Х. Лим и др. как индикатор метаногенеза в водонасыщенных почвах. C. A. McCartney et al. использовали его как прокси для производства метана у крупного рогатого скота.
Между тем, он также используется, чтобы помочь понять древнюю биогеохимию. Ричард Д. Панкост и соавт. Использовали его в качестве биомаркера. с целью реконструкции биогеохимии голоцена на омбротрофных торфяниках. Пилотное исследование под руководством Яна Д. Булла и соавт. также использовали археол в качестве биомаркера, чтобы выявить различия между ферментирующими пищеварительными системами в передней кишке и задней кишке древних травоядных млекопитающих.
Кроме того, потому что Из-за различной кинетики деградации интактного археола и кальдархеола отношение археола к кальдархеолу было предложено в качестве показателя солености в высокогорных озерах, что послужило инструментом для изучения палеозасоленности.
Археол также может гидролизоваться в некоторых случаях, его боковые цепи сохраняются в виде фитана или пристана, в зависимости от окислительно-восстановительных условий.
Для анализа археол липиды обычно экстрагируют с помощью традиционной процедуры Блая-Дайера, обычно с последующим фракционированием (тонкослойной или колоночной хроматографией) и дериватизацией. Казухиро Демизу и др. И Садами Оцубо и др. предложены аналогичные процессы, включающие кислотную экстракцию Блая и Дайера, кислотную обработку и дериватизацию, при этом основные липиды, наконец, подвергаются хроматографии.
Для определения концентрации археола, присутствующего в образце, обычно используются хроматографические технологии, в том числе высокоэффективная жидкостная хроматография (HPLC), газовая хроматография (GC) и сверхкритическая жидкостная хроматография (SFC) с масс-спектрометрией (MS) часто применяется для облегчения идентификации.