Полифосфаты - это соли или сложные эфиры полимерных оксианионов образованный из тетраэдрических PO4(фосфат ) структурных единиц, связанных вместе посредством общих атомов кислорода. Полифосфаты могут иметь линейную или циклическую кольцевую структуру. В биологии сложные эфиры полифосфатов ADP и ATP участвуют в хранении энергии. Различные полифосфаты находят применение в связывании минералов в муниципальных водах, обычно присутствуя в концентрации от 1 до 5 частей на миллион. GTP, CTP и UTP также являются важными нуклеотидами. в синтезе белка, синтезе липидов и углеводном обмене соответственно. Полифосфаты также используются в качестве пищевых добавок, обозначенных E452 .
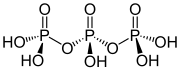
Структура трифосфорная кислота
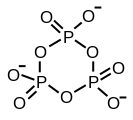
Циклический триметафосфат

Аденозиндифосфат (ADP)
Структура триполифосфорной кислоты иллюстрирует принципы, которые определяют структуры полифосфатов. Он состоит из трех тетраэдрических звеньев PO 4, связанных вместе посредством общих кислородных центров. Для линейных цепей концевые группы фосфора имеют один оксид, а остальные центры фосфора имеют два общих оксидных центра. Соответствующие фосфаты связаны с кислотами по потере кислых протонов. В случае циклического тримера каждый тетраэдр имеет две общие вершины со смежными тетраэдрами.
Возможно разделение трех углов. Этот мотив представляет собой сшивание линейного полимера. Сшитые полифосфаты имеют листовую структуру Филлосиликаты, но такие структуры возникают только в экстремальных условиях.
Полифосфаты возникают в результате полимеризации производных фосфорной кислоты. Процесс начинается с того, что две фосфатные единицы соединяются в реакции конденсации.
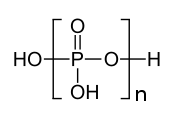
Конденсация показана как равновесие, поскольку обратная реакция, гидролиз, тоже возможно. Процесс может продолжаться поэтапно; на каждой стадии к цепи добавляется еще одно (PO 3) звено, как указано частью в скобках на иллюстрации полифосфорной кислоты. P 4O10можно рассматривать как конечный продукт реакций конденсации, где каждый тетраэдр имеет три общих угла с другими. И наоборот, сложная смесь полимеров образуется при добавлении небольшого количества воды к пятиокиси фосфора.
Полифосфаты - это слабые основания. Неподеленная пара электронов на атоме кислорода может быть отдана иону водорода (протону) или иону металла в типичном взаимодействии кислоты Льюиса - основания Льюиса. Это имеет огромное значение в биологии. Например, аденозинтрифосфат протонирован примерно на 25% в водном растворе при pH 7.
 6,6
6,6Происходит дальнейшее протонирование при более низких значениях pH.
АТФ образует хелатные комплексы с ионами металлов. Константа стабильности для равновесного
 4
4особенно велика. Образование комплекса магния является критическим элементом в процессе гидролиза АТФ, поскольку он ослабляет связь между концевой фосфатной группой и остальной частью молекулы.
Энергия, выделяемая при гидролизе АТФ,
при ΔG 
Полифосфаты с высокой молекулярной массой хорошо известны. Одним из производных является стекловидная (то есть аморфная) соль Грэма. Кристаллические полифосфаты с высоким молекулярным весом включают соль Куррола и соль Маддрелла. Эти частицы имеют формулу [NaPO 3]n[NaPO 3 (OH)] 2, где n может достигать 2000. С точки зрения их структуры, эти полимеры состоят из PO 3 «мономеры», цепи которых заканчиваются протонированными фосфатами.
Высокополимерные неорганические полифосфаты были обнаружены в живых организмах Л. Либерманом в 1890 г. Эти соединения представляют собой линейные полимеры, содержащие от нескольких до нескольких сотен остатков ортофосфата, связанных богатыми энергией фосфоангидридными связями.
Ранее он считался либо «молекулярным ископаемым», либо только источником фосфора и энергии, обеспечивающим выживание микроорганизмов в экстремальных условиях. В настоящее время известно, что эти соединения также выполняют регулирующую роль и встречаются у представителей всех царств живых организмов, участвуя в метаболической коррекции и контроле как на генетическом, так и на ферментативном уровнях. Полифосфат принимает непосредственное участие в переключении генетической программы, характерной для стадии экспоненциального роста бактерий, на программу выживания клеток в стационарных условиях, «жизнь в медленном движении». Они участвуют во многих регуляторных механизмах, встречающихся у бактерий:
Показано, что у человека полифосфаты играют ключевую роль в крови коагуляция. Вырабатываемые и высвобождаемые тромбоцитами, они активируют фактор свертывания крови фактор XII, который необходим для образования тромба. Фактор XII, также называемый фактором Хагемана, инициирует образование фибрина и выработку провоспалительного медиатора, брадикинина, который способствует утечке из кровеносных сосудов и тромбозу. Неорганические полифосфаты играют решающую роль в устойчивости дрожжевых клеток к токсичным катионам тяжелых металлов.
полифосфат натрия (E452 (i)), полифосфат калия (E452 (ii)), полифосфат натрия-кальция (E452 (iii)) и полифосфат кальция (E452 (iv)) используются в качестве пищевых добавок. Неизвестно, что они представляют какой-либо потенциальный риск для здоровья, кроме тех, которые обычно приписываются другим источникам фосфатов (включая те, которые встречаются в пище). Хотя высказывались опасения по поводу пагубного воздействия на кости и сердечно-сосудистых заболеваний, а также гиперфосфатемии, они кажутся актуальными только для чрезмерного потребления источников фосфатов. В целом разумное потребление (до 40 мг фосфата на кг массы тела в день) не представляет риска для здоровья.