| Исключенный домен катепсина С | |||||||||
|---|---|---|---|---|---|---|---|---|---|
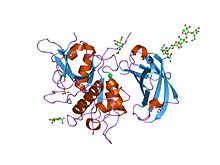 повторное определение нативной структуры дипептидилпептидазы i (катепсин с) человека повторное определение нативной структуры дипептидилпептидазы i (катепсин с) человека | |||||||||
| Идентификаторы | |||||||||
| Символ | CathepsinC_exc | ||||||||
| Pfam | PF08773 | ||||||||
| InterPro | IPR014882 | ||||||||
| SCOPe | 1k3b / SUPFAM | ||||||||
| |||||||||
Катепсин C (CTSC ), также известный как дипептидилпептидаза I (DPP-I ) представляет собой лизосомную экзо- цистеиновую протеазу, принадлежащую к семейству пептидаз C1. У человека он кодируется геном CTSC .
Катепсин C, по-видимому, является центральным координатором активации многих сериновых протеаз в иммунных / воспалительных клетках.
Катепсин C катализирует удаление дипептидов с N-конца белковых и пептидных субстратов, за исключением случаев, когда (i) аминогруппа N-конца заблокирована, (ii) сайт расщепления происходит по обе стороны от остатка пролина, (iii) N-концевой остаток представляет собой лизин или аргинин, или (iv) структура пептида или белка предотвращает дальнейшее расщепление с N-конца.
кДНК, кодирующие крысу, человека, мышь, бык, собаку и два шистосомы катепсина Cs, были клонированы и секвенированы и показали, что фермент является высококонсервативным. КДНК катепсина C человека и крысы кодируют предшественники (препрокатепсин C), содержащие сигнальные пептиды из 24 остатков, про-области из 205 (катепсин C) или 206 (катепсин C человека) остатков и каталитические домены из 233 остатков, которые содержат каталитические остатков и на 30-40% идентичны зрелым аминокислотным последовательностям папаина и ряда других катепсинов, включая катепсины, B, H, K, L и S.
. Транслированный препрокатепсин C преобразуется в зрелый образуются по крайней мере за счет четырех отщеплений полипептидной цепи. Сигнальный пептид удаляется во время транслокации или секреции профермента (прокатепсина C), а большой N-концевой фрагмент прорегиона (также известный как домен исключения), который сохраняется в зрелом ферменте, отделяется от каталитического домен путем вырезания минорной С-концевой части про-области, называемой активационным пептидом. Тяжелая цепь из примерно 164 остатков и легкая цепь из примерно 69 остатков образуются в результате расщепления каталитического домена.
В отличие от других членов семейства папаина, зрелый катепсин C состоит из четырех субъединиц, каждая из которых состоит из N-концевого фрагмента прорегиона, тяжелой цепи и легкой цепи. И про-фрагмент области, и тяжелая цепь гликозилированы.
Было показано, что дефекты кодируемого белка являются причиной болезни Папийона-Лефевра, аутосомно-рецессивного заболевания, характеризующегося ладонно-подошвенным кератозом и пародонтит.
Катепсин C функционирует как ключевой фермент в активации сериновых пептидаз гранул в воспалительных клетках, таких как эластаза и катепсин G в нейтрофильных клетках и химаза и триптаза в тучных клетках. При многих воспалительных заболеваниях, таких как ревматоидный артрит, хроническая обструктивная болезнь легких (ХОБЛ), воспалительное заболевание кишечника, астма, сепсис и муковисцидоз, значительная часть патогенеза обусловлена повышенной активностью некоторых из этих воспалительных протеаз. После активации катепсином С протеазы способны разрушать различные компоненты внеклеточного матрикса, что может привести к повреждению тканей и хроническому воспалению.