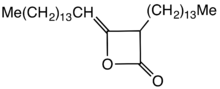
 структура AKD, полученная из пальмитиновой кислоты
структура AKD, полученная из пальмитиновой кислоты Димеры алкилкетена (AKD) являются семейством органические соединения на основе 4-членной кольцевой системы оксетан-2-она, которая также является центральным структурным элементом пропиолактона и дикетена. К оксетановому кольцу технически значимых димеров алкилкетена присоединена C 12 - C 16алкильная группа в 3-положении и C 13 - C 17 в 4 позиции.
Основное применение димеров алкилированного кетена - это проклейка бумаги и картона, а также гидрофобизация волокна целлюлозы. Модифицированные таким образом продукты отличаются более высокой механической прочностью и меньшим проникновением воды, чернилами или печатными красками.
особенностью AKD гидрофобные алкильные группы, простирающиеся от бета -пропиолактон кольцо. Конкретный пример получен из димеризации кетена стеариновой кислоты. Этот кетен образуется при пиролизе стеароилхлорида. AKD реагируют с гидроксильными группами на целлюлозе посредством реакции этерификации. Этерификация конкурирует с гидролизом AKD. До разработки AKD гидрофобность была придана путем включения в бумагу канифоли.
Связанным с AKD является ангидрид алкенилянтарной кислоты (ASA). Что касается AKD, ASA реагирует с гидроксигруппами целлюлозы с образованием сложного эфира, закрепляющего гидрофобную группу на поверхности. ASA получают по реакции ена непредельных углеводородов с малеиновым ангидридом.
Еще в 1901 году Эдгар Ведекинд опубликовал синтез алкила димеры кетена реакцией хлоридов карбоновой кислоты с третичными аминами, продуктами реакции полимеров.
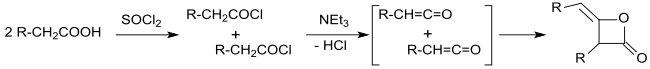
Молекулярная масса, определенная ранними исследователями, действительно указывает на кратность группы R 1R2CH = C = O. Поэтому в качестве продукта реакции был предложен так называемый пиронон (структура дикетона с циклобутановым кольцом ), т.е. г. из реакции изобутирилхлорида и триэтиламина.

Продукты первичной реакции хлорангидридов карбоновой кислоты с атомами водорода в α-положении и третичными аминами были идентифицированы Германом Штаудингером и Норманом Томасом Мортимером Уилсмором как высокореактивные кетены (этеноны), которые образуют 2-оксетаноны с алкилиденовой группой при димеризации в [2 + 2] фотоциклоприсоединения. Это постепенно внесло ясность в состав димеров алкилированного кетена.
Прояснение строения осложнялось различными продуктами димеризации кетенов. Например, простой кетен (H 2 C = C = O) димеризуется в дикетен (4-метилен-оксетан-2-он), в то время как замещенные кетены, такие как диметилкетен (Me 2 C = C = O, образованный из изобутирилхлорида с триэтиламином) димеризуется при последовательном присоединении к.
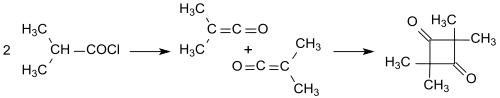
2,2,4,4,4-тетраметилциклобутандион может быть легко изомеризован в димер диметилкетена. (4-изопропилиден-3,3-диметилоксетан-2-он).

Синтез и характеристика димера гексадецилкетена, ключевого вещества для алкилированных димеров кетена, используемых в бумажной промышленности, были впервые описаны в патенте в 1945 г. и в публикации 1947 г.
Квантово-химическое исследование отклонило образование циклобутандиона во время димеризации н-алкилкетена R-CH = C = O в пользу образования более термодинамически более стабильного оксетана. Структура -2-он.
Промышленный синтез алкилированных кетенедимеров (в то время еще называемых кетоэтенонами) был запатентован в 1945 году из длинноцепочечной карбоновой кислоты. хлориды цид в инертных растворителях (таких как диэтиловый эфир или бензол ) с триэтиламином в качестве третичного амина в безводных условиях. После фильтрации нерастворимого гидрохлорида триэтиламина и выпаривания растворителя получают димеры с длинной цепью алкила с выходами более 90%.
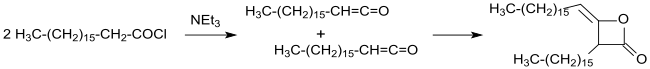
Использование других растворителей, таких как сложные эфиры карбоновой кислоты или кетоны для более легкого разделения гидрохлоридов триалкиламина или других аминов, таких как N, N, N ', N'-тетраметил-гексан-1,6-диамин, не дает каких-либо значительных преимуществ.
Также описаны процессы без использования растворителя, в которых образующийся гидрохлорид амина либо отфильтровывают, либо экстрагируют разбавленными водными кислотами.
Непрерывный процесс, в котором хлорид длинноцепочечной карбоновой кислоты и третичный амин (например, диметилизопропиламин, диметилциклогексиламин или триэтиламин) подается отдельно без растворителей в трубчатый реактор, месильную машину или, предпочтительно, двухшнековый экструдер или планетарный валковый экструдер, и реагирует при температурах от 90 до 110 ° C, обеспечивает содержание лактона более 90% за короткое время реакции. Обработка осуществляется посредством разделения фаз или кислотной экстракции.
Проблемы, связанные с кислотным (опосредованным сульфатом алюминия) проклеиванием массы бумаги с переваренной щелочью колониевой смолой, представленной с начала 19 века, помимо использования щелочных флокулянтов (таких как мел или карбонат кальция в качестве резерва щелочи) к поиску альтернативных материалов для проклейки в нейтральной или щелочной среде. В дополнение к значительно более реакционноспособным ангидридам алкенилянтарной кислоты (которые также быстро гидролизуются в присутствии воды) алкилированные димеры кетена начали быть предпочтительными поверхностными и массовыми размерами в бумажной промышленности с 1960-х годов, начиная с 1950-е годы.

Промышленно применяемые AKD получают из жирных кислот с длиной цепи от C14 (миристиновая кислота ) до C22 (бегеновая кислота ); Предпочтительно используют пальмитил (C16) дикетен и стеарил (C18) кетен и их смеси, а также смеси жирных кислот, полученные в результате гидролиза животных и растительных жиров. Из-за длины цепи исходных жирных кислот AKD представляют собой воскообразные твердые вещества с температурой плавления от 42 до примерно 70 ° C. Смеси димеров алкилированного кетена и воды представляют собой дисперсии при температурах ниже 40 ° C или эмульсии при температурах выше 45 ° C. Жидкие AKD широко не используются, они основаны на ненасыщенных жирных кислотах, таких как олеиновая кислота, или разветвленных жирных кислотах, таких как изостеариновая кислота.
Водные дисперсии алкилдикетена обычно содержат 10-20 мас.% AKD, а также активные защитные коллоиды (в частности, поликатионы, такие как катионный крахмал, сополимеры N-винилпирролидона и кватернизованный N-винилимидазол, ацилированные полиэтиленимины или катионные высокомолекулярные полиакриламиды со средней молярной массой до 7 миллионов г / моль) и другие стабилизаторы (обычно анионные поверхностно-активные вещества, например лигнинсульфонаты или продукты конденсации натриевой соли нафталинсульфоновой кислоты и формальдегида ). Такие стабилизированные дисперсии AKD активны и стабильны при комнатной температуре до трех месяцев, а также допускают добавление различных наполнителей для бумаги или картона (например, каолин, мел, тальк, диоксид титана, сульфат кальция, оксид алюминия и др.) От 5 до 25%. Количества димеров алкилкетена, используемых для проклейки бумаги и бумажных изделий, предпочтительно находятся в диапазоне от 0,15 до 0,8 мас.%, Иногда от 0,05 до 0,2 мас.% В расчете на сухую бумажную массу.
Для проклейки бумаги с помощью AKD был предложен трехэтапный процесс, который, несмотря на противоречивые дискуссии в 1990-х годах, кажется, лучше всего описывает процессы, которые происходят и объясняет достигнутые результаты. Решающими критериями качества гидрофобности бумаги являются

Молекулярная структура (т. е. молярная масса и степень сшивки), молярная плотность заряда катионных групп, точная дозировка катионного полимера в качестве стабилизатора дисперсии и удерживающей добавки, а также соблюдение других параметров процесса, таких как температура, pH и время пребывания. ключевой.
После удаления избытка воды - также во избежание гидролиза AKD до бета-кетокислоты и последующего декарбоксилирования до кетона -

следует за крекингом стабилизированных частиц AKD на бумажная масса-основа, плавление твердого воска AKD (примерно при 90 ° C), распространение жидкого воска AKD посредством поверхностной диффузии на целлюлозных волокнах и образование замкнутых гидрофобных слоев. Толщина гидрофобных слоев зависит от концентрации АКД в дисперсии.
Ad 3. Гидрофобизация целлюлозных волокон алкилированными димерами кетена наиболее эффективно протекает в нейтральной или предпочтительно слабощелочной среде (pH 7,5-9,0).. Температура реакции обычно составляет 90-110 ° C, при этом примерно 40% используемого AKD реагирует с целлюлозой. После реакции измеряют краевые углы >100 °, что указывает на гидрофобный характер модельных поверхностей, модифицированных AKD. Этерификация гидроксильных групп целлюлозных волокон также была продемонстрирована путем сравнения реакций с C-меткой AKD.
Проклейка с AKD подходит для постоянной гидрофобизации газетной, печатной и писчей бумаги и картон, используемый в качестве контейнера для жидкостей (в том числе пищевых продуктов, таких как молоко), а также для улучшения стабильности формы и текучести.