 | |
| Имена | |
|---|---|
| Другие имена Сульфат таллия, сульфат таллия | |
| Идентификаторы | |
| Номер CAS | |
| 3D-модель (JSmol ) | |
| ChemSpider | |
| ECHA InfoCard | 100.028.365 |
| KEGG | |
| PubChem CID | |
| UNII | |
| CompTox Dashboard (EPA ) | |
InChI
| |
УЛЫБКА
| |
| Свойства | |
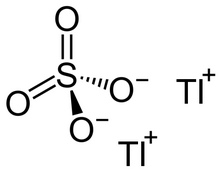
| Химическая формула | Tl2SO4 |
| Молярная масса | 504,83 г / моль |
| Внешний вид | белые призмы или плотный белый порошок |
| Запах | без запаха |
| Плотность | 6,77 г / см |
| Температура плавления | 632 ° C (1170 ° F; 905 K) |
| Растворимость в воде | 2,70 г / 100 мл (0 ° C). 4,87 г / 100 мл (20 ° C). 18,45 г / 100 мл (100 ° C) |
| Магнитная восприимчивость (χ) | -112,6 · 10 см / моль |
| Показатель преломления (nD) | 1,860 |
| Структура | |
| Кристаллическая структура | ромбовидная |
| Опасности | |
| Классификация ЕС (DSD) (устаревшее) | |
| R-фразы (устаревшие) | R28, R38, R48 / 25,. R51 / 53 |
| S-фразы (устаревшие) | (S1 / 2), S13, S36 / 37,. S45, S61 |
| NFPA 704 (огненный алмаз) |  0 4 0 0 4 0 |
| Смертельная доза или концентрация (LD, LC): | |
| LD50(средняя доза ) | 16 мг / кг (крыса, перорально). 23,5 мг / кг (мышь, перорально) |
| Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобокс | |
сульфат таллия (I) (Tl2SO4) или сульфат таллия представляет собой сульфат соль таллия в обычном состоянии окисления +1, как показано римская цифра I. Его часто называют просто таллий су lfate.
В течение последних двух столетий Т1 2SO4использовался для различных медицинских процедур, но от него отказались. В конце 1900-х годов он нашел применение в основном для родентицидов. Эти применения были запрещены в 1975 году в США из-за неселективной природы его токсичности. Сульфат таллия (I) подавляет рост растений, предотвращая прорастание. Tl 2SO4сегодня в основном используется в качестве источника Tl в исследовательских лабораториях. Он является предшественником сульфида таллия (I) (Tl 2 S), который проявляет высокую электрическую проводимость при воздействии инфракрасного света.
Сульфат таллия (I) получают реакцией металлического таллия с серной кислотой с последующей кристаллизацией.
Tl2SO4принимает та же структура, что и K 2SO4. В водном растворе катионы таллия (I) и сульфатные анионы разделены и сильно сольватированы. Кристаллы сульфата таллия (I) имеют симметрию C 2.
Сульфат таллия (I) растворим в воде, и его токсические эффекты обусловлены катионом таллия (I). Средняя смертельная доза сульфата таллия (I) для взрослого человека составляет около 1 грамма. Поскольку сульфат таллия (I) представляет собой простой порошок с неотличимыми свойствами, его можно легко принять за более безвредные химические вещества. Он может попасть в организм при проглатывании, вдыхании или при контакте с кожей. Катион таллия (I) очень похож на катионы калия и натрия, которые необходимы для жизни. После того, как ион таллия попадает в клетку, многие процессы транспорта калия и натрия нарушаются. Из-за его ядовитой природы многие западные страны запретили использование сульфата таллия (I) в продуктах для домашнего использования, и многие компании также прекратили использование этого соединения.
Дозировка свыше 500 мг считается смертельной. Сульфат таллия (I) после попадания в организм концентрируется в почках, печени, головном мозге и других тканях организма.
Сульфат таллия (I) использовался в Израиле для борьбы с популяцией грызунов; есть подозрение, что в 1950-х годах это привело к исчезновению бурая рыба-сова.