 | |
 | |
| Клинические данные | |
|---|---|
| Торговые наименования | Инвираза, Фортоваза |
| AHFS / Наркотики.com | Монография |
| MedlinePlus | a696001 |
| Данные лицензии |
|
| Беременность. категория |
|
| Код ATC | |
| Юридический статус | |
| Юридический статус |
|
| Фармакокинетические данные | |
| Биодоступность | ~ 4% (без повышения ритонавира ) |
| Белок связывание | 98% |
| Метаболизм | Печень, в основном за счет CYP3A4 |
| период полувыведения | 9–15 часов |
| Выведение | кал (81%) и моча ( 3%) |
| Идентификаторы | |
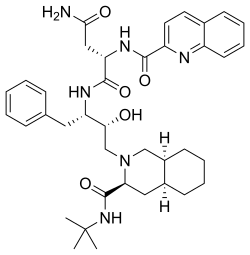
Название ИЮПАК
| |
| Номер CAS | |
| PubChem CID | |
| IUPHAR / BPS | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| KEGG | |
| ChEMBL |
|
| NIAID ChemDB | |
| CompTox Dashboard (EPA ) | |
| Химические и физические данные | |
| Формула | C38H50N6O5 |
| Молярная масса | 670,855 г · моль |
| 3D мес. del (JSmol ) | |
УЛЫБКИ
| |
InChI
| |
Саквинавир (SQV ), продается под торговыми марками Invirase и Фортоваза - это антиретровирусный препарат, используемый вместе с другими лекарствами для лечения или профилактики ВИЧ / СПИДа. Обычно его используют с ритонавиром или лопинавиром / ритонавиром для усиления его эффекта. Его принимают внутрь.
Общие побочные эффекты включают тошноту, рвоту, диарею и чувство усталости. Более серьезные побочные эффекты включают проблемы с удлинением интервала QT, блокадой сердца, повышенным содержанием липидов в крови и проблемами с печенью. Это кажется безопасным во время беременности. Он относится к классу ингибиторов протеазы и действует, блокируя протеазу ВИЧ..
Саквинавир был запатентован в 1988 году и впервые продан в 1995 году.
Саквинавир используется вместе с другими лекарствами для лечения или профилактики ВИЧ / СПИДа. Обычно он используется с ритонавиром или лопинавиром / ритонавиром для усиления его эффекта.
Наиболее частые побочные эффекты саквинавира в любом препарата проявляются легкие желудочно-кишечные симптомы, включая диарею, тошноту, жидкий стул и дискомфорт в животе. Инвираза лучше переносится, чем фортоваза.
Саквинавир в составе инвиразы имеет низкую и непостоянную биодоступность при пероральном приеме при приеме отдельно. Состав Fortovase в стандартной дозировке обеспечивает примерно в восемь раз больше активного лекарственного средства, чем Invirase, также в стандартной дозировке.
В клинике было обнаружено, что пероральная биодоступность саквинавира в обеих формах значительно увеличивается, когда пациенты также получают ИП ритонавир. Для пациентов это имеет большое преимущество в том, что они могут принимать меньше саквинавира при сохранении достаточного уровня саквинавира в плазме крови для эффективного подавления репликации ВИЧ.
Механизм этого долгожданного наблюдения не был напрямую известен, но позже он Было определено, что ритонавир ингибирует изофермент цитохрома P450 3A4. Обычно этот фермент метаболизирует саквинавир до неактивной формы, но из-за того, что ритонавир ингибирует этот фермент, уровни саквинавира в плазме крови значительно увеличиваются. Кроме того, ритонавир также подавляет переносчики нескольких лекарственных препаратов, хотя и в гораздо меньшей степени.
В отличие от других ингибиторов протеазы, абсорбция саквинавира, по-видимому, улучшается за счет омепразола.
Саквинавир - ингибитор протеазы. Протеазы - это ферменты, которые расщепляют молекулы белка на более мелкие фрагменты. Протеаза ВИЧ жизненно важна как для репликации вируса в клетке, так и для высвобождения зрелых вирусных частиц из инфицированной клетки. Саквинавир связывается с активным центром вирусной протеазы и предотвращает расщепление вирусных полипротеинов, предотвращая созревание вируса. Саквинавир подавляет протеазы как ВИЧ-1, так и ВИЧ-2.
 Новые случаи ВИЧ-инфекции и смерти до и после утверждения FDA «высокоактивной антиретровирусной терапии», в том числе саквинавиром, ритонавиром и индинавиром. key в качестве первых трех ингибиторов протеаз. Калли, Меган (28 ноября 2018 г.). «Ингибиторы протеазы открывают путь комбинированной терапии». природа. Открытая публикация. Проверено 28 октября 2020 г. В результате применения новых методов лечения смертность от ВИЧ в Соединенных Штатах резко снизилась за два года.}}
Новые случаи ВИЧ-инфекции и смерти до и после утверждения FDA «высокоактивной антиретровирусной терапии», в том числе саквинавиром, ритонавиром и индинавиром. key в качестве первых трех ингибиторов протеаз. Калли, Меган (28 ноября 2018 г.). «Ингибиторы протеазы открывают путь комбинированной терапии». природа. Открытая публикация. Проверено 28 октября 2020 г. В результате применения новых методов лечения смертность от ВИЧ в Соединенных Штатах резко снизилась за два года.}} Саквинавир был разработан фармацевтической компанией Roche. Саквинавир был шестым антиретровирусным препаратом и первым ингибитором протеазы, одобренным Управлением по контролю за продуктами и лекарствами (FDA), опередив ритонавир и индинавир на несколько месяцев. Этот новый класс антиретровирусных препаратов сыграл решающую роль в разработке высокоактивной антиретровирусной терапии (ВААРТ), которая помогла значительно снизить риск смерти от причин, связанных со СПИДом, о чем свидетельствует снижение ежегодного показателя смертности от ВИЧ в США, с более чем 50 000 до примерно 18 000 в течение двух лет.
Рош запросил и получил одобрение Invirase через программу FDA «Accelerated Approval» - процесс, разработанный для ускорения вывода на рынок лекарств для лечения серьезных заболеваний - решение, которое было спорным, поскольку активисты СПИДа расходились во мнениях относительно преимуществ тщательного тестирования по сравнению с ранним доступом к новым лекарствам. 7 ноября 1997 года он был снова одобрен как Fortovase, мягкая гелевая капсула, измененная для улучшения биодоступности. В мае 2005 года компания Roche объявила, что, учитывая снижение спроса, Fortovase прекратит выпуск в начале 2006 года в пользу инвиразы, усиленной ритонавиром, из-за способности последнего комбинированного препарата ингибировать фермент, который метаболизирует лекарства от СПИДа.
По состоянию на 2015 год он недоступен в качестве дженерика и стоит дорого.
На рынке представлены два состава: