 | |
| Имена | |
|---|---|
| Систематическое название IUPAC Фениллитий | |
| Другие названия Фениллитий | |
| Идентификаторы | |
| Номер CAS | |
| 3D-модель (JSmol ) | |
| Сокращения | LiPh, PhLi |
| Ссылка Beilstein | 506502 |
| ChEBI | |
| ChemSpider | |
| ECHA InfoCard | 100.008.838 |
| Номер ЕС |
|
| Ссылка Gmelin | 2849 |
| MeSH | фениллитий |
| PubChem CID | |
| CompTox Dashboard (EPA ) | |
InChI
| |
УЛЫБКИ
| |
| Свойства | |
| Химическая формула | LiC. 6H. 5 |
| Молярная масса | 84,045 г моль |
| Внешний вид | Бесцветные кристаллы |
| Плотность | 828 мг / см |
| Температура кипения | от 140 до 143 ° C (от 284 до 289 ° F; От 413 до 416 K) |
| Растворимость в воде | Реагирует |
| Термохимия | |
| Стандартная энтальпия. образования (ΔfH298) | 48,3-52,5 кДж моль |
| Опасности | |
| Данные по безопасности лист | Внешний паспорт безопасности данных |
| R-фразы (устаревшие) | R14, R17, R23 / 24/25, R48 |
| S-фразы (устаревшие) | (S1 / 2), S8, S9, S16, S26, S30, S46, S36 / 37/39, S45 |
| Если не указано иное, данные приведены для материалов в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки ink | |
Фениллитий или литобензол представляет собой металлоорганический агент с эмпирической формулой C 6H5Li. Чаще всего он используется в качестве металлирующего агента в органическом синтезе и вместо реагентов Гриньяра для введения фенильных групп в органический синтез. Кристаллический фениллитий бесцветен; однако растворы фениллития имеют различные оттенки коричневого или красного в зависимости от используемого растворителя и примесей, присутствующих в растворенном веществе.
Фениллитий представляет собой литийорганическое соединение, которое образует моноклинные кристаллы. Твердый фениллитий можно описать как состоящий из димерных субъединиц Li 2Pdiv class="ht". Атомы Li и атомы углерода ипсо фенильных колец образуют плоское четырехчленное кольцо. Плоскость фенильных групп перпендикулярна плоскости этого кольца Li 2C2. Между этими димерами фениллития и π-электронами фенильных групп в соседних димерах возникает дополнительная прочная межмолекулярная связь, в результате чего образуется бесконечная полимерная лестничная структура.
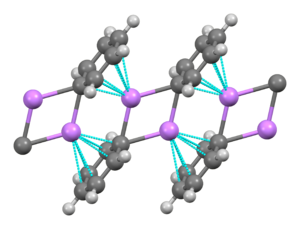
В растворе требуется множество структур, зависящих от органического растворителя. В тетрагидрофуране он находится в равновесии между состояниями мономера и димера. В обычном эфире фениллитий существует в виде тетрамера. Четыре атома Li и четыре углеродных центра ipso занимают чередующиеся вершины искаженного куба. Фенильные группы находятся на гранях тетраэдра и связаны с тремя ближайшими атомами Li.
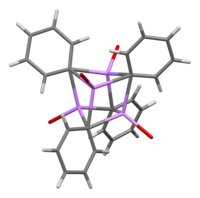
Длина связи C – Li составляет в среднем 2,33 Å. Молекула эфира связывается с каждым из участков Li через атом кислорода. В присутствии LiBr, побочного продукта прямой реакции лития с фенилгалогенидом, комплекс [(PhLi • Et 2O)4] вместо этого превращается в [(PhLi • Et 2O)3• LiBr). Атом Li в LiBr занимает один из литиевые центры в кластере кубанового типа и атом Br находится в соседнем углеродном центре.
Фениллитий впервые был получен реакцией металлического лития с дифенилртуть :
Взаимодействие фенилгалогенида с металлическим литием дает фениллитий:
Фениллитиевый может также могут быть синтезированы с помощью реакции обмена металл-галоген:
Преобладающим методом получения фениллития сегодня являются два последних синтеза.
Основное использование PhLi состоит в том, чтобы способствовать образованию углерод-углеродных связей посредством реакций нуклеофильного присоединения и замещения:
2-Фенилпиридин получают по реакции f фениллитий с пиридином, процесс, который влечет за собой путь присоединения-отщепления: