 Бис (триметилсилил) амидный лиганд, присоединенный к металлическому центру M.
Бис (триметилсилил) амидный лиганд, присоединенный к металлическому центру M. Бис (триметилсилил) амиды металлов (часто сокращенно называемые силиламидами металлов) представляют собой координационные комплексы, состоящие из катионного металла с анионными бис (триметилсилил) амидными лигандами, и являются частью более широкой категории амидов металлов.
Из-за объемного углеводородного скелета бис (триметилсилил) амидные комплексы металлов имеют низкую энергию решетки и являются липофильными. По этой причине они растворимы в ряде неполярных органических растворителей, в отличие от простых галогенидов металлов, которые растворяются только в реакционноспособных растворителях. Эти пространственные объемные комплексы являются молекулярными, состоящими из моно-, ди- и тетрамеров. Имея встроенную основу, эти соединения удобно реагируют даже с слабо протонными реагентами. Класс лигандов и новаторские исследования их координационных соединений были описаны Бюргером и Ваннагатом.
Лиганды часто обозначают как hmds (например, M (N (SiMe 3) 2) 3 = M (hmds) 3) в отношении гексаметилдисилазана, из которого они получены.
Помимо комплексов групп 1 и 2, общий способ получения бис (триметилсилил) амидов металлов включает реакции безводного хлорида металла с бис (триметилсилил) амидами щелочных металлов посредством реакции метатезиса солей :
Хлорид щелочного металла, образующийся в качестве побочного продукта, обычно осаждается в виде твердого вещества, что позволяет удалить его фильтрацией. Оставшийся бис (триметилсилил) амид металла затем часто очищают перегонкой или сублимацией.
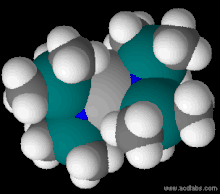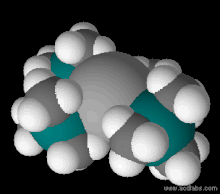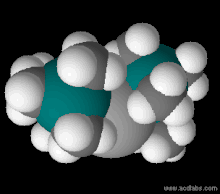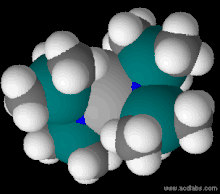 Модель заполнения пространства Fe [N (SiMe 3) 2 ] 2. Цветовая гамма: H - белый, Fe - серый, N - синий (едва заметный), Si - сине-зеленый.
Модель заполнения пространства Fe [N (SiMe 3) 2 ] 2. Цветовая гамма: H - белый, Fe - серый, N - синий (едва заметный), Si - сине-зеленый. Бис (триметилсилил) амиды лития, натрия и калия коммерчески доступны. В отсутствие растворителя комплексы лития и натрия являются тримерными, а комплекс калия - димерными в твердом состоянии. Литиевый реагент может быть приготовлен из н-бутиллития и бис (триметилсилил) амина :
Также описана прямая реакция этих расплавленных металлов с бис (триметилсилил) амином при высокой температуре:
Силиламиды щелочных металлов растворимы в ряде органических растворителей, где они существуют в виде агрегатов, и обычно используются в органической химии в качестве сильных стерически затрудненных оснований. Они также широко используются в качестве предшественников для синтеза других бис (триметилсилил) амидных комплексов (см. Ниже).
Комплексы кальция и бария могут быть получены обычным способом путем обработки йодида кальция или хлорида бария бис (триметилсилил) амидом калия или натрия. Однако этот метод может привести к загрязнению калием. Улучшенный синтез, включающий реакцию бензилкалия с иодидом кальция, с последующей реакцией с бис (триметилсилил) амином, приводит к материалу, не содержащему калия:
Силиламиды магния можно получить из дибутилмагния ; который коммерчески доступен в виде смеси изомеров n-Bu и s-Bu. Он депротонирует свободный амин с образованием бис (триметилсилил) амида магния, который сам коммерчески доступен.
В отличие от металлов группы 1, амин NH в бис (триметилсилил) амине недостаточно кислый, чтобы реагировать с металлами группы 2, однако комплексы могут быть получены посредством реакции бис (триметилсилил) амида олова (II) с соответствующим металлом.:
Для этого синтеза требуется длительное время реакции, и когда его проводят в присутствии координирующих растворителей, таких как диметоксиэтан, образуются аддукты. Следовательно, для получения свободных комплексов необходимо использовать некоординирующие растворители, такие как бензол или толуол.
Бис (триметилсилил) амид олова (II) получают из безводного хлорида олова (II) и коммерчески доступны. Он используется для получения бис (триметилсилиламидов) других металлов путем трансметаллирования. Группы 13 и висмута (III), бис (триметилсилил) амиды, которые получают таким же образом; алюминиевый комплекс может быть также получен обработкой сильноосновного алюмогидрида лития исходным амином:
Альтернативный синтез тетранитрида тетрасеры включает использование бис (триметилсилил) амида металла [(Me 3 Si) 2 N] 2 S в качестве предшественника с предварительно образованными связями S – N. [(Me 3 Si) 2 N] 2 S получают реакцией бис (триметилсилил) амида лития и дихлорида серы (SCl 2).
Бис (триметилсилил) амид металла [((CH 3) 3Si) 2N] 2S реагирует с комбинацией SCl 2 и сульфурилхлорида (SO 2 Cl 2) с образованием S 4 N 4, триметилсилилхлорида и диоксида серы:
Тетранитрид тетраселена, Se 4 N 4, представляет собой соединение, аналогичное тетранитриду тетрасеры, и его можно синтезировать реакцией тетрахлорида селена с [((CH 3) 3Si) 2N] 2Se. Последнее соединение представляет собой бис (триметилсилил) амид металла и может быть синтезировано реакцией тетрахлорида селена (SeCl 4), монохлорида селена ( Se 2Cl 2) и бис (триметилсилил) амид лития.
 Замороженный бис (триметилсилил) амид цинка. Это соединение плавится при 12,5 ° C.
Замороженный бис (триметилсилил) амид цинка. Это соединение плавится при 12,5 ° C.  Трис {бис (триметилсилил) амид} титана (слева) и ванадия (справа).
Трис {бис (триметилсилил) амид} титана (слева) и ванадия (справа). В соответствии с общим методом, бис (триметилсилил) амиды переходных металлов получают реакцией между галогенидами металлов (обычно хлоридами) и бис (триметилсилил) амидом натрия, однако существуют некоторые вариации, например, синтез синего Ti ( N (SiMe 3) 2) 3 с использованием растворимого предшественника TiCl 3 ( Et 3 N ) 3. Температуры плавления и кипения комплексов снижаются по мере роста ряда, при этом металлы группы 12 являются достаточно летучими, чтобы их можно было очистить дистилляцией.
Комплексы железа примечательны тем, что они изолированы как в состояниях окисления двухвалентного (II), так и трехвалентного (III). Fe [N (SiMe 3) 2 ] 3 может быть получен обработкой трихлорида железа бис (триметилсилил) амидом лития и является парамагнитным, поскольку высокоспиновое железо (III) содержит 5 неспаренных электронов.
Точно так же двухкоординированный комплекс Fe [N (SiMe 3) 2 ] 2 получают обработкой дихлорида железа бис (триметилсилил) амидом лития:
 Трис {бис (триметилсилил) амид железа}
Трис {бис (триметилсилил) амид железа} Темно-зеленый комплекс Fe [N (SiMe 3) 2 ] 2 существует в двух формах в зависимости от его физического состояния. При комнатной температуре соединение представляет собой мономерную жидкость с двухкоординатными центрами Fe, обладающими симметрией S 4, в твердом состоянии образует димер с тригональными плоскими центрами железа и мостиковыми амидогруппами. Низкое координационное число комплекса железа в значительной степени обусловлено стерическими эффектами объемного бис (триметилсилил) амида, однако комплекс будет связывать ТГФ с образованием аддукта {(THF) Fe [N (SiMe 3) 2 ] 2 }. Аналогичное поведение можно наблюдать в Mn (hmds) 2 и Co (hmds) 2, которые являются мономерными в газовой фазе и димерными в кристаллической фазе. Комплексы группы 11 особенно склонны к олигомеризации с образованием тетрамеров в твердой фазе. Сообщалось о кислотных свойствах Льюиса комплексов группы 12, а улучшенные числа E и C для комплексов Zn и Cd перечислены в модели ECW.
| Сложный | Появление | т.пл. (° C) | т.кип (° C) | Вращение | Комментарий |
|---|---|---|---|---|---|
| Комплексы 3-й группы | |||||
| Сбн (hmds) 3 | Бесцветное твердое вещество | 172–174 | S = 0 | ||
| Y (hmds) 3 | Белое твердое вещество | 180–184 | 105 ° C / 10 мм рт. Ст. (Субл.) | S = 0 | В продаже |
| Комплексы 4-й группы | |||||
| Ti (hmds) 3 | Ярко-синее твердое вещество | S = 1/2 | Получен из TiCl 3 (N (CH 3) 3) 2 | ||
| Комплексы 5-й группы | |||||
| V (hmds) 3 | Темно-фиолетовое твердое вещество | 174–176 | S = 1 | Получен из VCl 3 (N (CH 3) 3) 2 | |
| Комплексы 6-й группы | |||||
| Cr (hmds) 3 | Яблочно-зеленый твердый | 120 | 110 / 0,5 мм рт. Ст. (Субл.) | S = 3/2 | |
| Комплексы 7-й группы | |||||
| Mn (hmds) 2 | Бежевый твердый | 100 / 0,2 мм рт. | S = 5/2 | ||
| Mn (hmds) 3 | Фиолетовый твердый | 108-110 | S = 2 | ||
| Комплексы 8-й группы | |||||
| Fe (hmds) 2 | Светло-зеленое твердое вещество | 90-100 / 0,01 мм рт. | |||
| Fe (hmds) 3 | Темно-зеленое твердое вещество | 120 / 0,5 мм рт. Ст. (Субл.) | S = 5/2 | ||
| Комплексы 9 группы | |||||
| Co (hmds) | Черный твердый | Тетрамерика в твердом состоянии | |||
| Co (hmds) 2 | Зеленое твердое вещество | 73 | 101 / 0,6 мм рт. | ||
| Co (hmds) 3 | Темно-оливково-зеленое твердое вещество | 86-88 | S = 2 | ||
| Комплексы 10-й группы | |||||
| Ni (hmds) | Черный твердый | gt; 250 | Тетрамерика в твердом состоянии | ||
| Ni (hmds) 2 | Красная жидкость | 80 / 0,2 мм рт. | |||
| Комплексы 11 группы | |||||
| Cu (hmds) | Бесцветное твердое вещество | 180 / 0,2 мм рт. Ст. (Субл.) | S = 0 | ||
| Ag (hmds) | Бесцветное твердое вещество | S = 0 | Нерастворим в углеводородах и диэтиловом эфире. | ||
| Au (hmds) | Бесцветное твердое вещество | S = 0 | |||
| Комплексы 12 группы | |||||
| Zn (hmds) 2 | Бесцветная жидкость | 12,5 | 82 / 0,5 мм рт. | S = 0 | В продаже |
| CD (hmds) 2 | Бесцветная жидкость | 8 | 93 / 0,5 мм рт. | S = 0 | |
| Hg (hmds) 2 | Бесцветная жидкость | 11 | 78 / 0,15 мм рт. | S = 0 | |
Трифлаты лантаноидов могут быть удобными безводными предшественниками многих бис (триметилсилил) амидов:
Однако более распространено получение бис (триметилсилил) амидов лантаноидов из безводных хлоридов лантаноидов, поскольку они дешевле. Реакция проводится в ТГФ и требует периода кипячения с обратным холодильником. После образования продукт отделяется от LiCl путем замены растворителя на толуол, в котором Ln (hmds) 3 растворим, а LiCl - нет.
Силиламиды важны в качестве исходных материалов в химии лантаноидов, поскольку хлориды лантаноидов имеют либо плохую растворимость, либо плохую стабильность в обычных растворителях. В результате этого почти все силиламиды лантаноидов коммерчески доступны.
| Сложный | Появление | т.пл. (° C) | Комментарий |
|---|---|---|---|
| La (hmds) 3 | белый | 145-149 | |
| Ce (hmds) 3 | Желто-коричневый | 132–140 | |
| Pr (hmds) 3 | Бледно-зеленый | 155-158 | |
| Nd (hmds) 3 | Бледно-синий | 161–164 | |
| Sm (hmds) 3 | Палевый | 155-158 | |
| Eu (hmds) 3 | апельсин | 159–162 | |
| Gd (hmds) 3 | белый | 160–163 | |
| Dy (hmds) 3 | Бледно-зеленый | 157–160 | |
| Ho (hmds) 3 | Кремовый цвет | 161–164 | |
| Yb (hmds) 3 | Желтый | 162–165 | |
| Лу (hmds) 3 | белый | 167–170 |
Также был достигнут некоторый успех в синтезе и изучении актинид-бис (триметилсилил) амидов. В удобном способе синтеза в качестве исходных материалов используются THF-аддукты йодидных солей AnI 3 (THF) 4.
| Сложный | Появление | т.пл. (° C) | Комментарий |
|---|---|---|---|
| U (hmds) 3 | Красно-пурпурный | 137–140 | Сублимирует при 80-100 ° C ( ок 10 -3 торр) |
| Np (hmds) 3 | Голубовато-черный | Сублимирует при температуре 60 ° C ( ок 10 -4 Торр) | |
| Pu (hmds) 3 | Желто-оранжевый | Сублимирует при температуре 60 ° C ( ок 10 -4 Торр) |
Бис (триметилсилил) амиды металлов являются сильными основаниями. Они вызывают коррозию и несовместимы со многими хлорированными растворителями. Эти соединения бурно реагируют с водой, и с ними следует обращаться безвоздушным способом.