 Связывание кислорода с простетической группой гема, которая будет частью гемопротеина.
Связывание кислорода с простетической группой гема, которая будет частью гемопротеина. Гемопротеины (или haemprotein ; также гемо- или haemoprotein), или гем белки, представляет собой белка, который содержит гем протезной группы. Это очень большой класс металлопротеинов. Гемовая группа обеспечивает функциональность, которая может включать перенос кислорода, восстановление кислорода, перенос электронов и другие процессы. Гем связан с белком либо ковалентно, либо нековалентно, либо и тем, и другим.
Гема состоит из железа, связанный катиона в центре сопряженного основания в порфирине, а также других лигандов, присоединенный к «продольным участкам» из железа. Порфириновое кольцо представляет собой плоский дианионный тетрадентатный лиганд. Железо обычно представляет собой Fe 2+ или Fe 3+. На аксиальных участках прикреплены один или два лиганда. Порфириновое кольцо имеет 4 атома азота, которые связываются с железом, оставляя два других координационных положения железа доступными для связывания с гистидином белка и двухвалентным атомом.
Гемепротеины, вероятно, эволюционировали, чтобы включить атом железа, содержащийся в протопорфириновом IX кольце гема, в белки. Поскольку он заставляет гемепротеины реагировать на молекулы, которые могут связывать двухвалентное железо, эта стратегия сохранялась на протяжении всей эволюции, поскольку он выполняет важные физиологические функции. Кислород (O 2), оксид азота (NO), монооксид углерода (CO) и сероводород (H 2 S) связываются с атомом железа в гемовых белках. После связывания с простетическими гемовыми группами эти молекулы могут модулировать активность / функцию этих гемопротеинов, обеспечивая передачу сигнала. Поэтому при производстве в биологических системах (клетках) эти газообразные молекулы называются газопередатчиками.
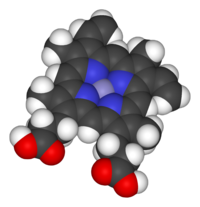 Модель из Fe- протопорфирина IX субъединицей Гем B кофактора.
Модель из Fe- протопорфирина IX субъединицей Гем B кофактора. Из-за их разнообразных биологических функций и широкого распространения гемепротеины являются одними из наиболее изученных биомолекул. Данные о структуре и функции гемового белка были собраны в The Heme Protein Database (HPD), вторичной базе данных для Protein Data Bank.
Сенсорная система также опирается на некоторых гемопротеинах включая FixL, датчик кислорода, СООА, датчик моноксида углерода, и растворимый гуанилатциклазы.
Гемоглобин и миоглобин являются примерами гемопротеинов, которые соответственно транспортируют и хранят кислород у млекопитающих. Гемоглобин - это четвертичный белок, который встречается в красных кровяных тельцах, тогда как миоглобин - это третичный белок, обнаруженный в мышечных клетках млекопитающих. Хотя они могут различаться по расположению и размеру, их функции аналогичны. Оба гемопротеина содержат простетическую группу гема.
His-F8 миоглобина, также известный как проксимальный гистидин, ковалентно связан с 5-м координационным положением железа. Кислород взаимодействует с дистальным His посредством водородной связи, а не ковалентной. Он связывается с 6-м координационным положением железа, His-E7 миоглобина связывается с кислородом, который теперь ковалентно связан с железом. То же самое и с гемоглобином; однако, будучи белком с четырьмя субъединицами, гемоглобин в целом содержит четыре гемовых единицы, что позволяет четырем молекулам кислорода в общей сложности связываться с белком.
Миоглобин и гемоглобин - это глобулярные белки, которые служат для связывания и доставки кислорода с помощью простетической группы. Эти глобины значительно улучшают концентрацию молекулярного кислорода, который может переноситься в биологических жидкостях позвоночных и некоторых беспозвоночных.
Различия возникают в связывании лиганда и аллостерической регуляции.
Миоглобин содержится в мышечных клетках позвоночных. Приведенные в действие мышечные клетки могут быстро нуждаться в большом количестве кислорода для дыхания из-за их энергетических потребностей. Следовательно, мышечные клетки используют миоглобин для ускорения диффузии кислорода и действуют как локальные запасы кислорода во время интенсивного дыхания. Миоглобин также сохраняет необходимое количество кислорода и делает его доступным для митохондрий мышечных клеток.
У позвоночных гемоглобин находится в цитозоле красных кровяных телец. Гемоглобин иногда называют белком, транспортирующим кислород, чтобы противопоставить его миоглобину, который является стационарным.
У позвоночных кислород поступает в организм тканями легких и передается эритроцитам в кровотоке. Затем кислород распределяется по всем тканям тела и выгружается из красных кровяных телец в дышащие клетки. Затем гемоглобин улавливает углекислый газ, который возвращается в легкие. Таким образом, гемоглобин связывает и разгружает кислород и углекислый газ в соответствующих тканях, служа для доставки кислорода, необходимого для клеточного метаболизма, и удаления образующегося отхода, CO 2.
Цитохром с оксидаза - это фермент, встроенный во внутреннюю мембрану митохондрий. Его основная функция - окислять белок цитохрома с. Цитохром с оксидаза содержит несколько активных центров металлов.
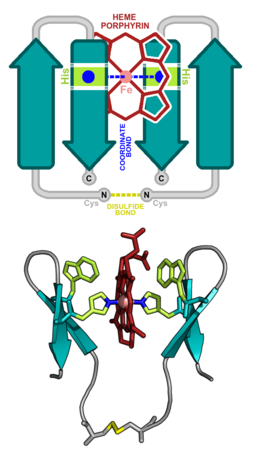 Pincer-1 [1] : разработанный гем-связывающий пептид, имеющий полностью бета-вторичную структуру. Вверху: Топологическое представление Pincer-1, показывающее вторичную структуру и сконструированные взаимодействующие остатки. НИЖЕ: Трехмерная модель Pincer-1, состоящая из атомов. Эта модель была частично подтверждена с помощью ЯМР.
Pincer-1 [1] : разработанный гем-связывающий пептид, имеющий полностью бета-вторичную структуру. Вверху: Топологическое представление Pincer-1, показывающее вторичную структуру и сконструированные взаимодействующие остатки. НИЖЕ: Трехмерная модель Pincer-1, состоящая из атомов. Эта модель была частично подтверждена с помощью ЯМР. Благодаря разнообразию функций молекулы гема: как переносчик электронов, переносчик кислорода и как кофактор фермента, связывающие гем белки постоянно привлекают внимание разработчиков белков. Первоначальные попытки дизайна были сосредоточены на α-спиральных гемосвязывающих белках, отчасти из-за относительной простоты конструирования самособирающихся спиральных пучков. Сайты связывания гема были сконструированы внутри межспиральных гидрофобных бороздок. Примеры таких конструкций включают:
Более поздние попытки проектирования были сосредоточены на создании функциональных спиральных связок гема, таких как:
Методы конструирования достигли такой степени зрелости, что теперь возможно создавать целые библиотеки гемсвязывающих спиральных белков [18].
Недавние попытки разработки были сосредоточены на создании полностью связывающих бета-гем белков, новая топология которых очень редко встречается в природе. К таким конструкциям относятся: