| Альфа-цепь термолабильного энтеротоксина | |||||||||
|---|---|---|---|---|---|---|---|---|---|
 холотоксин, кристаллическая форма 1 холотоксин, кристаллическая форма 1 | |||||||||
| Идентификаторы | |||||||||
| Условное обозначение | Энтеротоксин_а | ||||||||
| Pfam | PF01375 | ||||||||
| Клан пфам | CL0084 | ||||||||
| ИнтерПро | IPR001144 | ||||||||
| Объем | 1л / СУПФАМ | ||||||||
| |||||||||
| Бета-цепь термолабильного энтеротоксина | |||||||||
|---|---|---|---|---|---|---|---|---|---|
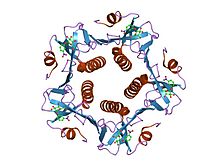 b-пентамер холерного токсина в комплексе с метанитрофенил-альфа-d-галактозой b-пентамер холерного токсина в комплексе с метанитрофенил-альфа-d-галактозой | |||||||||
| Идентификаторы | |||||||||
| Условное обозначение | Энтеротоксин_b | ||||||||
| Pfam | PF01376 | ||||||||
| ИнтерПро | IPR001835 | ||||||||
| Объем | 1л / СУПФАМ | ||||||||
| |||||||||
| Термолабильный энтеротоксин типа II, субъединица B (LT-IIB) | |||||||||
|---|---|---|---|---|---|---|---|---|---|
 Escherichia coli термолабильный энтеротоксин b-пентамер типа iib Escherichia coli термолабильный энтеротоксин b-пентамер типа iib | |||||||||
| Идентификаторы | |||||||||
| Условное обозначение | LT-IIB | ||||||||
| Pfam | PF06453 | ||||||||
| ИнтерПро | IPR010503 | ||||||||
| Объем | 1tii / СУПФАМ | ||||||||
| |||||||||
В молекулярной биологии, то термолабильный энтеротоксин семейство включает в себя кишечной палочки термолабильный энтеротоксин (ELT или LT) и холерный токсин (СТХ), секретируемый холерного вибриона.
Он назван так потому, что инактивируется при высоких температурах.
Субъединица A транспортируются внутрь пентамерными субъединицами B. Затем он действует, повышая уровни цАМФ за счет ADP-рибозилирования альфа-субъединицы Gs-белка, что приводит к конститутивной активации аденилатциклазы. Повышенные уровни цАМФ стимулируют активацию CFTR канала, таким образом, стимулирующего секрецию хлорида ионов и воды из энтероцитов в кишечнике просвет. Этот ионный дисбаланс вызывает водянистую диарею.
В дополнение к своим эффектам на секрецию хлоридов, которые включают те же этапы, что и действие токсина холеры, Elt связывает дополнительные субстраты: липополисахарид на поверхности клеток E. coli и антигены крови A-типа. Важность этих обязывающих событий пока не известна.
Эти токсины состоят из мультимерной структуры AB5, в которой пентамер цепей B выполняет мембранно-связывающую функцию, а цепь A необходима для ферментативной активности. Субъединицы B расположены в виде пентамера в форме пончика, каждая субъединица участвует в ~ 30 водородных связях и 6 солевых мостиках со своими двумя соседями.
Субъединица A имеет менее четко выраженную вторичную структуру. Это преимущественно взаимодействует с пентамером через фрагмент A2 C-концевой, которая проходит через центральную заряженную пору из B субъединиц. Предполагаемый каталитический остаток во фрагменте A1 (Glu112) находится рядом с гидрофобной областью, которая объединяет две петли вместе. Считается, что эта область может быть важна для катализа и транслокации мембран.
Структурная организация термолабильных энтеротоксинов E. coli типа I и типа II очень похожа, хотя антигенно различается.
Токсин холеры переносится бактериофагом CTXφ и может быть выделен из пламид. E.coli, LT (ELT) аналогичным образом связан с подвижными элементами, в данном случае Ent плазмид, которые могут нести LT, ST, или обоих. Последовательности частичной вставки (IS), фланкирующие гены elt, обеспечивают дополнительные возможности передачи за счет гомологичной рекомбинации в их инвертированных повторах. Также описана индуцированная Aβ-фагом конверсия в E. coli.
Субъединицы B токсинов этого семейства относительно безвредны сами по себе. CtxB обычно используется в качестве нейронального индикатора. Elt-IB рассматривался как адъювант в трансдермальных вакцинах.