Адсорбируемые органические галогениды (AOX) - это мера содержания органических галогенов в месте отбора проб, например, в почве из отходы свалки, воды или сточных вод. Эта процедура определяет хлор, бром и йод как эквивалентные галогены, но не измеряет уровни фтора в образце.
Использование галогенсодержащих материалов в таких процессах, как очистка воды, отбеливание или даже общий синтез для создания конечного продукта, образуется ряд органических галогенидов. Эти органические галогениды выбрасываются со сточными водами нефтяной, химической и бумажной промышленности и попадают к потребителю, а затем на свалки или океанические свалки. Внутри почвы соединения гало сопротивляются разложению и часто вступают в реакцию с ионами металлов, в результате чего образуются неразлагаемые комплексы металлов, повышается токсичность почвы и накапливается в пищевой цепи водных организмов. До 2000 ppm этих биоаккумулятивных органических хлоридов было обнаружено в жире рыбы из вод, куда отбеливающие стоки сбрасывались бумажными фабриками, где концентрация воды в 2% считается токсичной для рыбы. Хотя строгие правительственные постановления позволили снизить высокий уровень выбросов в прошлом, эти соединения попадают в источники воды из-за неправильной утилизации потребителями предметов, содержащих хлорированные соединения. Наличие любых органических галогенидов в природной воде считается признаком загрязнения ксенобиотиками. Попадая в воду, встречающиеся в природе фульвокислоты и гуминовые кислоты могут приводить к образованию мутагенных соединений, таких как галогенированный фуранон MX (Z-3-хлор-4 - (дихлорметил) -5-гидрокси-2 (5H) -фуранон). Употребление этих мутагенных соединений может вызвать несколько аномалий в развитии и воспроизводстве у людей из-за длительного периода полураспада и имитации рецепторов гормонов. Например, такие соединения, как диоксины, могут ингибировать действие половых гормонов за счет связывания со стероидными рецепторами, вызывая длительное разрушение клеток в нескольких тканях.
Стойкие органические загрязнители, такие как дихлордифенилтрихлорэтан (ДДТ), полихлорированные бифенолы, диоксины, все оцениваются с помощью анализа AOX. Как правило, чем выше количество хлора в органическом соединении, тем оно считается более токсичным. Хотя существует несколько биохимических или электрохимических методов удаления органических галогенидов, предпочтение отдается АОХ из-за его низкой стоимости эксплуатации и простоты конструкции.
В лаборатории определение параметра АОХ состоит из адсорбции органических галогенидов. от образца к активированному углю. Активированный уголь может быть порошкообразным или гранулированным и адсорбироваться с использованием микроколонок или периодического процесса, если образцы богаты гуминовыми кислотами. В случае периодического процесса часто используется интенсивное встряхивание, чтобы способствовать адсорбции органического галогенида на активированном угле из-за его электроотрицательности и наличия неподеленных пар. Неорганические галогениды, которые также адсорбируются, вымываются сильной кислотой, такой как азотная кислота. Уголь с адсорбированным органическим галогенидом получают фильтрованием, после чего фильтр, содержащий уголь, сжигают в присутствии кислорода. При сгорании углеводородной части соединений образуются CO 2 и H 2 O, галогеновые кислоты образуются из галогенов. Эти галогенкислоты поглощаются уксусной кислотой. Последующее использование микроколуметрического титрования, электрохимического метода количественного определения, позволяет определить содержание АОХ в образце. Используя коэффициент разбавления, можно оценить общее содержание АОХ на участке. В качестве альтернативы, хлорированные соединения в образце можно определить с помощью пентановой экстракции с последующей капиллярной газовой хроматографией и захватом электронов (GC-ECD ). Органический углерод, оставшийся после продувки азотной кислотой, можно анализировать, используя влажное окисление персульфатом УФ с последующим инфракрасным детектированием (ИК ). Некоторые другие аналитические методы, такие как высокоэффективная жидкостная хроматография (ВЭЖХ), также могут быть применены для количественного определения уровней АОХ. Общая процедура адсорбции приведена ниже:
Где 


На водоочистных установках органические галогениды адсорбируются с помощью GAC или PAC в резервуарах с мешалкой. Наполненный углерод отделяется с помощью мембраны, изготовленной из таких материалов, как полипропилен или нитрат целлюлозы. Измерение уровней АОХ в зоне обработки и за ее пределами показывает падение концентрации органических галогенидов. В некоторых процессах используется двухступенчатая фильтрация GAC для удаления предшественников AOX и, таким образом, уменьшения количества AOX в очищенной воде. Двухступенчатый процесс фильтрации состоит из двух последовательно соединенных фильтров GAC. В первый фильтр загружается отработанный GAC, а во второй фильтр - свежий GAC. Такая установка предпочтительна из-за ее повышенной эффективности и пропускной способности. GAC заменяется циклически, а затем извлеченная смесь галогенида и углерода направляется на последующую биологическую или химическую обработку, такую как озонирование, для регенерации GAC. Часто эти химические обработки, хотя и эффективны, создают экономические проблемы для очистных сооружений.
Более экономически привлекательным вариантом обработки органических галогенидов является использование биологических агентов. В последнее время бактерии (Ancylobacter aquaticus), грибы (Phanerochaete chrysosporium и Coiriolus versicolor) или синтетические ферменты использовались для разложения хлорированных органических соединений. Микроорганизмы разлагают галогенсодержащие соединения с использованием аэробных или анаэробных процессов. Механизмы разложения включают использование соединения в качестве источника углерода для получения энергии, кометаболита или в качестве акцептора электронов. Обратите внимание, что ферментативное или микробное действие можно регулировать посредством ингибирования с обратной связью - конечный продукт в серии подавляет реакцию в процессе. Пример микроба, который может разлагать AOX, показан ниже на рисунках 1 и 2.
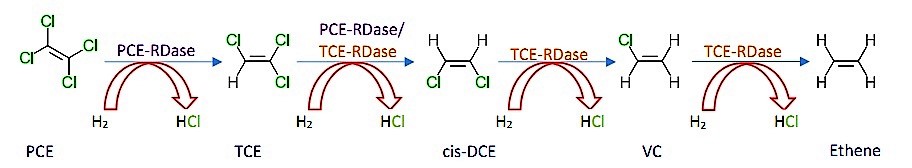 Рисунок 1: Поэтапное разложение PCE
Рисунок 1: Поэтапное разложение PCE Образец дехлорирования хлорированных алифатических углеводородов (CAH), таких как перхлорэтилен (PCE) от Dehalococcoides ethenogenes проиллюстрировано выше. PCE - один из сильно хлорированных CAH, в котором отсутствуют известные микроорганизмы, способные к аэробному разложению. Высокий электроотрицательный характер PCE обеспечивает способность окислителя за счет принятия электронов путем совместного метаболизма или дегалоидыхания. При совместном метаболизме снижение PCE становится возможным за счет использования первичного метаболита для получения углерода и источника энергии. При дегалогенодыхании перенос электронов от окисления малых молекул (H 2 является основным источником; но также можно использовать глюкозу, ацетат, формиат и метанол) к PCE генерирует энергию, необходимую для роста бактерий. Водород, участвующий в этом механизме, часто является продуктом другого процесса, такого как ферментация простых молекул, таких как сахара, или других сложных молекул, таких как жирные кислоты. Более того, из-за конкуренции со стороны метаногенов за H 2, дехлорирующие бактерии предпочитают низкие концентрации H 2, и часто достигаются за счет соединений ферментации с медленным высвобождением, таких как в виде жирных кислот и разлагающейся бактериальной биомассы. В то время как несколько ферментов и переносчиков электронов участвуют в процессе, два фермента выполняют реакции дехлорирования - редуктивная дегидрогеназа PCE (PCE-RDase) и TCE-редуктивная дегидрогеназа (TCE-RDase). PCE-RDase обычно свободно находится в цитоплазме, в то время как TCE-RDase находится прикрепленной к внешней цитоплазматической мембране. Эти ферменты обычно используют кластер ионов металла, такой как кластер Fe-S, для завершения цикла переноса электрона. Водород окисляется с образованием двух протонов и двух электронов. Удаление первого хлорида, которое выполняется PCE-RDase, восстанавливает PCE до TCE путем восстановительного дегалогенирования, когда гидрид заменяет хлор. Хлорид, потерянный из PCE, приобретает два электрона и протон, который их сопровождает, с образованием HCl. TCE может быть восстановлен до цис-дихлорэтилена (цис-DCE) с помощью PCE-RDase или TCE-RDase. Последующее восстановление до винилхлорида (VC) и этилена выполняется с помощью TCE-RDase. Дехлорирование PCE до цис-DCE происходит быстрее и термодинамически более выгодно, чем дехлорирование цис-DCE до VC. Превращение ВК в этилен является самой медленной стадией процесса и, следовательно, ограничивает общую скорость реакции. Скорость восстановительного дехлорирования также напрямую коррелирует с количеством атомов хлора и, как таковая, уменьшается с уменьшением количества атомов хлора. Кроме того, в то время как несколько групп бактерий, таких как Desulfomonile, Dehalobacter, Desulfuromonas... и т. Д. может выполнить дегалогенирование PCE до TCE, только группа Dehalococcoides может выполнить полное восстановительное дехлорирование от PCE до этена.
 Рис. 2: 2,4,6- Разложение ТБФ под действием Ochrobactrum sp. основано на работе Yamada et al., 2008.
Рис. 2: 2,4,6- Разложение ТБФ под действием Ochrobactrum sp. основано на работе Yamada et al., 2008. Сообщалось, что помимо дехлорирования CAH, микробы также действуют на хлорированные ароматические углеводороды. Пример реакции, в которой содержание ароматических АО снижается, показан на рисунке 2 выше. Хотя мало что известно о механизмах дегалогенирования полигалогенированных фенолов (PHP) и полигалогенированных бензолов (PHB), наблюдалась региоселективность в отношении расположения галогенидов на ароматическом кольце. Однако в этой региоселективности доминируют как окислительно-восстановительные потенциалы реакции, так и знакомство микробов с реакцией. Более того, из-за специфичности большинства микробов наряду со сложными ароматическими структурами, для достижения полного дегалогенирования используется смесь более чем одного вида бактерий и / или грибов (часто называемая консорциумом). Реакция на фиг. 2 показывает восстановительное дебромирование 2,4,6-трибромфенола (2,4,6-ТБФ) с помощью Ochrabactrum. На основании относительной деградации молекулы наряду с аналитическими результатами было постулировано, что разложение 2,4,6-ТБФ протекает через дебромирование ортоброма на первой стадии дегалогеназой с образованием 2,4- дибромфенол (2,4-ДБФ). Поскольку существует два орто-брома, дебромирование любого из ортоуглеродов дает один и тот же продукт. Другие виды, такие как Pseudomonas galthei или Azotobacter sp., продемонстрировали предпочтение пара-галогенидов над мета- или орто-галогенидами. Например, Azotobacter sp. разлагает 2,4,6-трихлорфенол (2,4,6-TCP) до 2,6-дихлоргидрохинона из-за селективности TCP-4-монооксигеназы. различия между орто- и пара-галогенидом. Эти различия в региоселективности между видами можно объяснить специфичностью трехмерной структуры фермента и ее препятствием для стерических взаимодействий. Было высказано предположение, что протон теряется фенольной группой 2,4,6-ТБФ, что приводит к образованию отрицательно заряженного галогенфенолят-иона. Последующая атака пара-углерода гидрид-анионом из NAD (P) H путем нуклеофильной атаки и резонансной перегруппировки приводит к замещению брома гидридом и образованию 2,4-ДБФ. Последующие стадии по аналогичной схеме дают 2-бромфенол и фенол на последней стадии. Фенол может метаболизироваться микроорганизмами с образованием метана и двуокиси углерода или может быть извлечен легче, чем AOX.
Органические галогениды, (EOX) и (TOX) являются связанными материалами для этой темы. EOX предоставляет информацию о том, как можно экстрагировать галогениды с помощью растворителя, в то время как TOX предоставляет информацию об общем содержании органических галогенидов в образце. Это значение можно использовать для оценки биохимической потребности в кислороде (BOD) или химической потребности в кислороде (COD), ключевого фактора при оценке количества кислорода, необходимого для сжигания органических соединений, для оценки процентного содержания АОХ и экстрагируемых органических галогенидов.