Трогоцитоз
редактировать
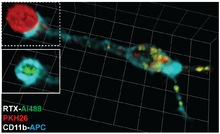
Объемная реконструкция из конфокальных срезов интерфейса клеток Ramos-RAW. Покрытые RTX-Al488 (зеленые), меченные PKH26 клетки Ramos (красные) инкубировали с клетками RAW в течение 45 минут при 37 ° C. Клетки RAW метили анти-CD11b-APC (голубой). Клетка RAW в значительной степени подверглась трогоцитозу как RTX, так и PKH26. На вставке показана пунктирная область над ней без наложения канала PKH26, показывающая концентрацию RTX-Al488 на интерфейсе ячейка-ячейка, в противном случае истощенная по сравнению с остальной частью ячейки Рамоса. Реакцию трогоцитоза останавливали фиксацией через 45 мин после совместной инкубации. Клетки Ramos имеют диаметр примерно 12 мкм.
Троцитоз (греч. : трого; грызть) - это процесс, при котором конъюгированы лимфоциты (B, T и NK клетки ) в антигенпрезентирующие клетки извлекают поверхностные молекулы из этих клеток и экспрессируют их на своей собственной поверхности. Молекулярная реорганизация, происходящая на границе между лимфоцитом и антигенпрезентирующей клеткой во время конъюгации, также называется «иммунологическим синапсом ».
Содержание
- 1 Шаги в открытии трогоцитоза
- 2 Типы клеток, выполняющих трогоцитоз
- 3 Механизмы трогоцитоза
- 4 Физиологические последствия
- 5 Влияние трогоцитоза в серотерапевтических подходах
- 6 Трогоцитоз методы иммуномониторинга
- 7 См. также
- 8 Ссылки
Этапы открытия трогоцитоза
Первые признаки существования этого процесса относятся к концу 70-х годов, когда несколько исследовательских групп сообщили о присутствие неожиданных молекул, таких как молекулы главного комплекса гистосовместимости (MHC), на Т-клетках. Представление о том, что фрагменты мембраны, а не изолированные молекулы, могут быть захвачены Т-клетками на антигенпрезентирующих клетках, было предложено путем захвата молекул MHC, слитых с зеленым флуоресцентным белком (GFP) в их внутриклеточной части. Доказательство того, что фрагменты мембраны участвуют в этом процессе переноса, было обнаружено, когда было обнаружено, что флуоресцентные зонды, встроенные в плазматическую мембрану антигенпрезентирующей клетки, а также молекулы, не являющиеся молекулами MHC, захватываются Т-клетками вместе с антигеном. 173>Типы клеток, осуществляющие трогоцитоз
Трогоцитоз первоначально был зарегистрирован в T-, B- и NK-клетках как in vivo, так и in vitro. На Т-клетках и В-клетках трогоцитоз запускается, когда Т-клеточный рецептор (TCR) на Т-клетках или В-клеточный рецептор (BCR) на В-клетках взаимодействует с антигеном, распознаваемым на антигенпрезентирующих клетках. Как и в лимфоцитах, трогоцитоз возникает с PMN (полиморфноядерные лейкоциты, также известные как гранулоциты) и связан с эффективным ADCC (цитотоксичность, опосредованная антителами).
Было показано, что для того, чтобы инициировать ADCC in vitro, PMN должны прилипать к своим клеткам-мишеням и образовывать плотные соединения с опсонизированными опухолевыми клетками антител. Эта кластеризация клеток предшествует взаимному обмену липидов мембраны между эффекторной и клеткой-мишенью во время ADCC и не происходит в отсутствие опсонизирующих антител. Трогоцитоз также встречается в моноцитах и дендритных клетках. За пределами иммунной системы подобный перенос мембранных фрагментов был зарегистрирован между спермой и ооцитами, процесс, который, как считается, способствует слиянию гамет.
В последнее время этот термин приписывают макрофагам, таким как резидентная микроглия ЦНС, которая способны частично фагоцитозировать части синапсов как часть процесса ремоделирования.
Механизмы трогоцитоза
Троцитоз включает перенос фрагментов плазматической мембраны от представляющей клетки к лимфоцит. Трогоцитоз специфически запускается сигналом рецептора антигена на Т- и В-клетках, ингибирующим киллером и активирующим киллером рецептором на NK-клетках и различными рецепторами на других клетках, включая рецептор Fc и рецептор скавенджера класса А. Вероятно, что трогоцитоз не включает захват везикул, таких как экзосомы, секретируемые антигенпрезентирующими клетками. Скорее, молекулы могут перемещаться от антигенпрезентирующих клеток к лимфоцитам, транспортируемым мембранными нанотрубками, или фрагменты мембран могут быть разорваны Т-клетками из-за физических сил, необходимых для образования и деформации иммунологических синапсов. В зависимости от двух типов клеток, участвующих в конъюгатах, трогоцитоз может быть однонаправленным или двунаправленным. Белков, переносимых посредством трогоцитоза, много, и в основном они включают белки, встроенные в плазматическую мембрану или тесно связанные с ней (белки, охватывающие липидный бислой или вставленные во внеклеточные или внутриклеточные листочки). Например, недавно было показано, что лимфоциты человека приобретают белок внутренней мембраны H-Ras, G-белок, жизненно важный для общих функций лимфоцитов и видный участник рака человека по сканируемым ими клеткам. Перенос был зависимым от клеточного контакта и происходил в контексте образования клеточного конъюгата. Более того, приобретение онкогенного H-RasG12V NK- и T-лимфоцитами имело важные биологические функции в адоптирующих лимфоцитах: перенесенный H-RasG12V индуцировал фосфорилирование ERK , усиление секреции интерферона-γ и фактора некроза опухоли-α , усиление пролиферации лимфоцитов и усиление NK-опосредованного уничтожения клеток-мишеней.
Физиологические последствия
Трогоцитоз может иметь физиологические последствия двумя способами: либо потому, что клетки-реципиенты приобретают и используют молекулы, которые они обычно не экспрессируют, либо потому, что «донорские» клетки лишены молекул., что может изменить их взаимодействие с клеточными партнерами. Приобретенные молекулы, например, с внеклеточными или внутриклеточными компонентами, могут изменять активность лимфоцитов и управлять несколькими функциями лимфоцитов, такими как миграция в адекватные поврежденные ткани. Такие полученные фрагменты плазматической мембраны также могут вносить вклад в способность пролиферировать, поскольку липиды являются высоко энергетическими компонентами, требующими создания. Трогоцитоз, возможно, впервые появился у очень примитивных организмов, чтобы питаться другими клетками. Большинство биологических функций, идентифицированных для трогоцитоза, было зарегистрировано для лимфоцитов и дендритных клеток. Основные выводы в этом направлении:
- цитотоксические Т-лимфоциты, захватившие комплексы антигенный пептид-MHC, могут быть убиты CTL, специфическими для этого антигена (процесс, называемый братоубийством)
- хелперный Т-лимфоцит, захвативший антигенный пептид-MHC комплексы участвуют в отрицательной регуляторной петле обратной связи, что приводит к их инактивации
- дендритные клетки, лишенные Т-клетками комплексов антигенный пептид-МНС в результате трогоцитоза, способствуют созреванию аффинности Т-клеточного ответа путем отбора высокоаффинных Т-клеток
- понижающая модуляция костимулирующих молекул на дендритных клетках, опосредованная Т-клетками, приводит к регуляции ответа Т-клеток.
- перенос антигена между дендритными клетками посредством трогоцитоза способствует реактивации Т-клеток памяти за счет наивные Т-клетки
- перенос антигена между дендритными клетками посредством трогоцитоза способствует отторжению аллотрансплантата
Влияние трогоцитоза на серотерапевтические подходы
Терапевтические антибактериальные препараты матрицы можно использовать для лечения рака. Примером может служить ритуксимаб, терапевтическое антитело, используемое для лечения хронического лимфоцитарного лейкоза, которое распознает молекулу CD20, экспрессируемую опухолевыми клетками, и приводит к их удалению. Однако использование слишком большого количества антитела частично связано с удалением комплексов ритуксимаб-CD20 с поверхности опухолевых клеток моноцитами посредством трогоцитоза. Этот эффект приводит к побегу клеток опухоли. Снижение дозы терапевтических антител для ограничения степени трогоцитоза может улучшить их терапевтическую эффективность.
Эпратузумаб (Mab CD22) действует, используя трогоцитоз, для переноса CD22 и других белков B-клеток от B-клеток к эффекторным клеткам. 118>
Анализы на основе трогоцитоза в качестве инструментов иммуномониторинга
Анализы TRAP (протокол анализа TRogocytosis) позволяют идентифицировать, характеризовать и очищать Т- и В-клетки, распознающие их специфический антиген, на основе их способности извлекать молекулы (в том числе случай, флуоресцентные зонды) из плазматической мембраны антигенпрезентирующих клеток. Для этих анализов требуется такое оборудование, как проточный цитометр, но в остальном они очень дешевы, просты в выполнении, быстрые (могут выполняться в течение 3 часов) и применимы к любой популяции Т- или В-клеток. Анализы TRAP были успешно использованы для обнаружения Т-клеточных ответов против вирусных инфекций, рака, аутоиммунных заболеваний и вакцин.
См. Также
Процесс трогоцитоза считается отличным от несвязанных процессов, но похож на них известные как фагоцитоз и парацитофагия.
Ссылки
- ^Joly, Etienne; Худризье, Дени (сентябрь 2003 г.). «Что такое трогоцитоз и каково его предназначение?». Иммунология природы. 4 (9): 815. doi : 10.1038 / ni0903-815. PMID 12942076.
- ^Huang, J.; Ян, Y; Sepulveda, H; Ши, Вт; Хван, я; Петерсон, Пенсильвания; Джексон, MR; Спрент, Дж; Цай, З. (29 октября 1999 г.). «TCR-опосредованная интернализация комплексов пептид-MHC, приобретенных Т-клетками». Наука. 286 (5441): 952–954. doi : 10.1126 / science.286.5441.952. PMID 10542149.
- ^Patel, Dhaval M.; Арнольд, Паула Й.; Белый, Грегори А.; Нарделла, Джон П.; Манни, Марк Д. (15 ноября 1999 г.). «Комплексы МНС / пептид класса II высвобождаются из APC и приобретаются Т-клеточными респондерами во время распознавания специфического антигена». Журнал иммунологии. 163 (10): 5201–5210. PMID 10553040.
- ^Худрисье, Денис; Рионд, Джоэлль; Мазаргиль, Оноре; Гэрин, Жан Эдуард; Жоли, Этьен (15 марта 2001 г.). «Передний край: CTL быстро захватывают мембранные фрагменты из клеток-мишеней зависимым от сигналов TCR способом». Журнал иммунологии. 166 (6): 3645–3649. doi : 10.4049 / jimmunol.166.6.3645. PMID 11238601.
- ^Хорнер, Хайке; Фрэнк, Карола; Dechant, Клаудиа; Репп, Роланд; Гленни, Мартин; Херрманн, Мартин; Штокмейер, Бернхард (1 июля 2007 г.). «Образование конъюгата интимных клеток и обмен мембранных липидов предшествуют индукции апоптоза в клетках-мишенях во время антителозависимой, опосредованной гранулоцитами цитотоксичности». Журнал иммунологии. 179 (1): 337–345. doi : 10.4049 / jimmunol.179.1.337. PMID 17579054.
- ^Барро-Ланж, Вирджиния; Науд-Барриан, Натали; Бомсель, Морган; Вольф, Жан-Филипп; Зийят, Ахмед (15 июня 2007 г.). «Перенос фрагментов мембран ооцита на оплодотворяющие сперматозоиды». Журнал FASEB. 21 (13): 3446–3449. doi : 10.1096 / fj.06-8035hyp. PMID 17575263.
- ^Вайнхард, Летиция; ди Бартоломей, Джулия; Боласко, Джулия; Мачадо, Педро; Schieber, Nicole L.; Нениските, Урте; Эксига, Мелани; Вадисиуте, Огюст; Раджоли, Анджело; Шертель, Андреас; Шваб, Янник; Гросс, Корнелиус Т. (26 марта 2018 г.). «Микроглия ремоделирует синапсы путем пресинаптического трогоцитоза и индукции филоподий головы позвоночника». Nature Communications. 9 (1): 1228. Bibcode : 2018NatCo... 9.1228W. DOI : 10.1038 / s41467-018-03566-5. PMC 5964317. PMID 29581545.
- ^Рехави, Одед; Гольдштейн, Итамар; Верницкий, Хелли; Ротблат, Барак; Клоог, Йоэль; Канеллопулос, Жан (21 ноября 2007 г.). «Межклеточная передача онкогенных H-Ras в иммунологическом синапсе». PLOS One. 2 (11): e1204. Bibcode : 2007PLoSO... 2.1204R. doi : 10.1371 / journal.pone.0001204. PMC 2065899. PMID 18030338.
- ^Хелфт, Джули; Жаке, Александра; Джонкер, Натали Т.; Гранжан, Изабель; Дороти, Гийом; Киссенпфенниг, Адриан; Малиссен, Бернар; Матцингер, Полли; Ланц, Оливье (15 августа 2008 г.). «Антиген-специфические Т-Т взаимодействия регулируют рост Т-лимфоцитов CD4». Кровь. 112 (4): 1249–1258. doi : 10.1182 / blood-2007-09-114389. PMC 2515122. PMID 18539897.
- ^Kedl, Ross M.; Шефер, Брайан Ч.; Капплер, Джон В.; Маррак, Филиппа (3 декабря 2001 г.). «Т-клетки подавляют комплексы пептид-MHC на APC in vivo». Иммунология природы. 3 (1): 27–32. doi : 10.1038 / ni742. PMID 11731800.
- ^Qureshi, Omar S.; Чжэн, Юн; Накамура, Киоко; Аттридж, Кесли; Манзотти, Клэр; Шмидт, Эмили М.; Бейкер, Дженнифер; Джеффри, Луиза Э.; Каур, Сатдип; Бриггс, Зоя; Hou, Tie Z.; Футтер, Клэр Э.; Андерсон, Грэм; Уокер, Люси С.К.; Сансом, Дэвид М. (29 апреля 2011 г.). «Трансэндоцитоз CD80 и CD86: молекулярная основа внешней функции клетки CTLA-4». Наука. 332 (6029): 600–603. Bibcode : 2011Sci... 332..600Q. doi : 10.1126 / science.1202947. PMC 3198051. PMID 21474713.
- ^Ваким, Линда М.; Беван, Майкл Дж. (31 марта 2011 г.). «Перекрестно одетые дендритные клетки управляют активацией CD8 + Т-клеток памяти после вирусной инфекции». Природа. 471 (7340): 629–632. Bibcode : 2011Natur.471..629W. DOI : 10.1038 / nature09863. PMC 3423191. PMID 21455179.
- ^Эррера, Оскель Баррозу; Гольшаян, Дела; Тибботт, Ребекка; Очоа, Франсиско Сальсидо; Джеймс, Марта Дж.; Marelli-Berg, Federica M.; Лехлер, Роберт И. (15 октября 2004 г.). «Новый путь презентации аллоантигена дендритными клетками». Журнал иммунологии. 173 (8): 4828–4837. doi : 10.4049 / jimmunol.173.8.4828. PMID 15470023.
- ^Beum, Paul V.; Кеннеди, Адам Д.; Уильямс, Майкл Э.; Линдорфер, Маргарет А.; Тейлор, Рональд П. (15 февраля 2006 г.). «Реакция на бритье: комплексы ритуксимаб / CD20 удаляются из клеток лимфомы мантийных клеток и клеток хронического лимфоцитарного лейкоза моноцитами THP-1». Журнал иммунологии. 176 (4): 2600–2609. doi : 10.4049 / jimmunol.176.4.2600. PMID 16456022.
- ^Уильямс, Майкл Э.; Денсмор, Джон Дж.; Pawluczkowycz, Andrew W.; Беум, Пол V.; Кеннеди, Адам Д.; Линдорфер, Маргарет А.; Hamil, Susan H.; Eggleton, Jane C.; Тейлор, Рональд П. (15 ноября 2006 г.). «Ритуксимаб в низких дозах трижды в неделю снижает потерю CD20 при бритье и способствует усиленному нацеливанию при хроническом лимфоцитарном лейкозе». Журнал иммунологии. 177 (10): 7435–7443. doi : 10.4049 / jimmunol.177.10.7435. PMID 17082663.
- ^«Эпратузумаб». Immunomedics.
- ^Добёф, Сандрин; Пуо, Анн-Лор; Жоли, Этьен; Худрисье, Дени (29 декабря 2006 г.). «Простой метод, основанный на трогоцитозе, для обнаружения, количественной оценки, характеристики и очистки антигенспецифических живых лимфоцитов с помощью проточной цитометрии путем захвата ими мембранных фрагментов антигенпрезентирующих клеток». Протоколы природы. 1 (6): 2536–2542. doi : 10.1038 / nprot.2006.400. PMID 17406507.
- ^Бидлинг, Кэрол; Слифка, Марк К. (1 октября 2006 г.). «Количественная оценка жизнеспособных вирус-специфических Т-клеток без априорного знания тонкой специфичности эпитопа». Природная медицина. 12 (10): 1208–1212. doi : 10,1038 / нм1413. PMID 17013384.
- ^Махленкин, Артур; Узана, Ронни; Франкенбург, Шошана; Айзенберг, Галит; Айзенбах, Леа; Питковски, Джейкоб; Городецкий, Рафаэль; Ниссан, Авирам; Перец, Тамар; Лотем, Михал (15 марта 2008 г.). «Захват мембран опухолевых клеток с помощью трогоцитоза способствует обнаружению и выделению опухолеспецифических функциональных CTL». Исследования рака. 68 (6): 2006–2013. DOI : 10.1158 / 0008-5472.CAN-07-3119. PMID 18339883.
- ^Bahbouhi, Bouchaib; Петре, Сеголен; Бертело, Лорелин; Гарсия, Александра; Элонг Нгоно, Энни; Дегаук, Николас; Мишель, Лор; Вертлевски, Сандрин; Лефрер, Фабьен; Мейниэль, Клэр; Делькруа, Екатерина; Бруар, Софи; Лаплауд, Давид-Аксель; Soulillou, Жан-Поль (июнь 2010 г.). «Распознавание Т-клетками аутоантигенпредставляющих клеток с помощью анализа переноса белка выявляет высокую частоту антимиелиновых Т-клеток при рассеянном склерозе». Мозг. 133 (6): 1622–1636. doi : 10.1093 / brain / awq074. PMID 20435630.
- ^Добёф, Сандрин; Превиль, Ксавье; Момот, Мари; Миссери, Иоланда; Жоли, Этьен; Худрисье, Дени (сентябрь 2009 г.). «Улучшение схем введения вакцин на основе CyaA с использованием анализов TRAP для обнаружения антиген-специфических CD8 + Т-клеток непосредственно ex vivo». Вакцина. 27 (41): 5565–5573. doi : 10.1016 / j.vaccine.2009.07.035. PMID 19647811.
 Объемная реконструкция из конфокальных срезов интерфейса клеток Ramos-RAW. Покрытые RTX-Al488 (зеленые), меченные PKH26 клетки Ramos (красные) инкубировали с клетками RAW в течение 45 минут при 37 ° C. Клетки RAW метили анти-CD11b-APC (голубой). Клетка RAW в значительной степени подверглась трогоцитозу как RTX, так и PKH26. На вставке показана пунктирная область над ней без наложения канала PKH26, показывающая концентрацию RTX-Al488 на интерфейсе ячейка-ячейка, в противном случае истощенная по сравнению с остальной частью ячейки Рамоса. Реакцию трогоцитоза останавливали фиксацией через 45 мин после совместной инкубации. Клетки Ramos имеют диаметр примерно 12 мкм.
Объемная реконструкция из конфокальных срезов интерфейса клеток Ramos-RAW. Покрытые RTX-Al488 (зеленые), меченные PKH26 клетки Ramos (красные) инкубировали с клетками RAW в течение 45 минут при 37 ° C. Клетки RAW метили анти-CD11b-APC (голубой). Клетка RAW в значительной степени подверглась трогоцитозу как RTX, так и PKH26. На вставке показана пунктирная область над ней без наложения канала PKH26, показывающая концентрацию RTX-Al488 на интерфейсе ячейка-ячейка, в противном случае истощенная по сравнению с остальной частью ячейки Рамоса. Реакцию трогоцитоза останавливали фиксацией через 45 мин после совместной инкубации. Клетки Ramos имеют диаметр примерно 12 мкм.