Войти
В серы Оксокислотах представляют собой химические соединения, которые содержат серу, кислород и водород. Наиболее известной и наиболее важной в промышленности является серная кислота. Сера содержит несколько оксокислот; однако некоторые из них известны только по их солям (они выделены курсивом в таблице ниже). Охарактеризованные кислоты содержат множество структурных особенностей, например:
| Кислота | Формула | Формальная степень окисления | Состав | Связанные анионы | Заметки |
|---|---|---|---|---|---|
| Серная кислота | H 2 SO 4 | +6 | 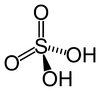 | Сульфат, SO 2- 4 и гидросульфат, широко известный как бисульфат, HSO - 4 | Самый известный и промышленно значимый. |
| Полисерные кислоты, включая дисерную кислоту или пиросерную кислоту | H 2 SO 4 n SO 3 | +6 | 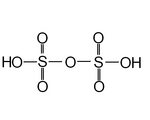 | Дисульфат (широко известный как пиросульфат ), S 2 О 2- 7 и трисульфат, S 3 О 2- 10 | Чистая дисерная кислота плавится при 36 ° C. Присутствует в дымящей серной кислоте, олеуме. Примеры известны для n = 1 и n = 2. |
| Пероксимоносерная кислота | H 2 SO 5 | +6 | 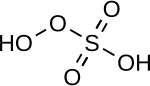 | Пероксомоносульфат, OOSO 2- 3 | «Кислота Каро», твердое вещество, плавящееся при 45 ° C. |
| Пероксидисерная кислота | H 2 S 2 O 8 | +6 | 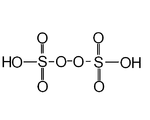 | Пероксидисульфат, O 3 SOOSO 2- 3 | «Кислота Маршалла», твердое вещество, плавление при 65 ° C. |
| Дитионовая кислота | H 2 S 2 O 6 | +5 |  | Дитионат, O 3 SSO 2- 3 | В чистом виде не изолирован, приготовлены только концентрированные растворы. |
| Тиосерная кислота | H 2 S 2 O 3 | 0 (для конечной серы), +4 (для центрального атома) | 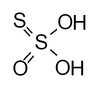 | Тиосульфат, S 2 О 2- 3 Гидрогентиосульфат HS 2 О - 3 (соль аммония, приготовленная в безводном метаноле при -80 ° C) | Водные растворы разлагаются. |
| Сернистая кислота или пиросернистая кислота | H 2 S 2 O 5 | +5 (атома серы, связанного с 3 атомами кислорода), +3 (другого атома серы) | 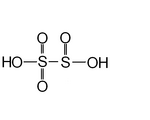 | Дисульфит, широко известный как метабисульфит, S 2 О 2- 5 | Неизвестный. |
| Сернистая кислота | H 2 SO 3 | +4 | 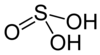 | Бисульфит, HSO - 3 и сульфит, SO 2- 3 | Неизвестный. |
| Дитионовая кислота | H 2 S 2 O 4 | +3 |  | Дитионит, O 2 SSO 2- 2 | Неизвестный. |
| Сульфоксиловая кислота | H 2 SO 2 | +2 | | Сульфоксилат, SO 2- 2 | Свободная кислота не известна |
| Политионовая кислота | H 2 S x O 6 | 0 (для мостиковых атомов S), +5 (для концевых центральных атомов S) |  | Политионаты, O 3 SS х −2 )ТАК 2- 3. Пример trithionate, тетратионат, pentathionate, hexathionate, heptathionate, octathionate, nonathionate, decathionate, undecathionate, dodecathionate, tridecathionate и tetradecathionate. | Примеры известны с x = 3, 4, 5, 6, 7, 8, 10, 12, 14. |
| Тиосерная кислота | H 2 S 2 O 2 | −1 (для внешнего атома серы), +3 (для центрального атома) | | Тиосульфиты | Неизвестный |
| Дигидроксидисульфан | H 2 S 2 O 2 | +1 | | Кислота известна |