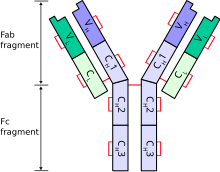
 Схематическая диаграмма типичного антитела показаны две тяжелые цепи Ig (синий), соединенные дисульфидными связями с двумя легкими цепями Ig (зеленый). Показаны константный (С) и вариабельный (V) домены.
Схематическая диаграмма типичного антитела показаны две тяжелые цепи Ig (синий), соединенные дисульфидными связями с двумя легкими цепями Ig (зеленый). Показаны константный (С) и вариабельный (V) домены. 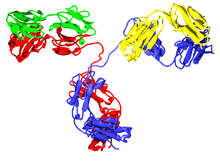 Молекула антитела. Две тяжелые цепи окрашены в красный и синий цвет, а две легкие цепи - в зеленый и желтый.
Молекула антитела. Две тяжелые цепи окрашены в красный и синий цвет, а две легкие цепи - в зеленый и желтый. Тяжелая цепь иммуноглобулина (IgH ) представляет собой большую полипептидную субъединицу антитело (иммуноглобулин). В геноме человека локусы гена IgH находятся на хромосоме 14.
Типичное антитело состоит из двух тяжелых цепей иммуноглобулина (Ig) и двух легких цепей Ig. Существует несколько различных типов тяжелой цепи, которые определяют класс или изотип антитела. Эти типы тяжелых цепей различаются у разных животных. Все тяжелые цепи содержат серию иммуноглобулиновых доменов, обычно с одним вариабельным доменом (VH), который важен для связывания антигена и нескольких константных доменов (C H 1, C H 2 и т. Д.). Производство жизнеспособной тяжелой цепи является ключевым этапом созревания В-клеток. Если тяжелая цепь способна связываться с суррогатной легкой цепью и перемещаться к плазматической мембране, тогда развивающаяся В-клетка может начать продуцировать свою легкую цепь.
Тяжелая цепь не всегда должна связываться с легкая цепь. Пре-В-лимфоциты могут синтезировать тяжелую цепь в отсутствие легкой цепи, что затем может позволить тяжелой цепи связываться со связывающим белком тяжелой цепи.
Существует пять типов тяжелой цепи иммуноглобулина млекопитающих: γ, δ, α, μ и ε. Они определяют классы иммуноглобулинов: IgG, IgD, IgA, IgM и IgE соответственно.
Каждая тяжелая цепь имеет две области:
Коровы, в частности Bos taurus, демонстрируют вариацию на общую тему млекопитающих, в которой участок CDR H3 тяжелой цепи адаптирован для получения разнообразного репертуара антител, которые представляют собой поверхность взаимодействия антигена «ножка и выступ» вместо более знакомой поверхности двухвалентного кончика. CDR крупного рогатого скота необычно длинная и содержит уникальные атрибуты последовательности, которые поддерживают продукцию парных цистеиновых остатков во время соматической гипермутации. Таким образом, если у людей стадия соматической гипермутации нацелена на процесс V (D) J-рекомбинации, то у коров целью является создание разнообразных дисульфидных связей и генерация уникальных наборов петли, которые взаимодействуют с антигеном. Предполагаемой эволюционной движущей силой этой вариации является наличие в пищеварительной системе коровы значительно более разнообразной микробной среды из-за того, что они являются жвачими животными.
Челюстные рыбы, по-видимому, являются самые примитивные животные, которые способны вырабатывать антитела, подобные описанным для млекопитающих. Однако у рыб нет такого же репертуара антител, как у млекопитающих. К настоящему времени у костистой рыбы.
Подобно ситуации, наблюдаемой для костистых рыб, у хрящевой рыбы идентифицированы три различных изотипа тяжелой цепи Ig. За исключением μ, эти изотипы тяжелой цепи Ig, по-видимому, являются уникальными для хрящевых рыб. Полученные антитела обозначаются как IgW (также называемые IgX или IgNARC) и IgNAR (рецептор нового антигена иммуноглобулина). Последний тип представляет собой антитело тяжелой цепи, антитело, лишенное легких цепей, и может быть использовано для получения однодоменных антител, которые по существу являются вариабельным доменом (V NAR) IgNAR. Однодоменные антитела акулы (V NAR s) к опухолевым или вирусным антигенам могут быть выделены из большой библиотеки V NAR акулы-няньки с использованием технологии фагового дисплея.
IgW имеет теперь также обнаружены в группе рыб с лопастными плавниками, включая латимерию и двоякодышащих рыб. IgW1 и IgW2 у целаканта имеют обычную (VD) структуру n-Jn-C, а также большое количество константных доменов.
лягушки могут синтезировать IgX и IgY.