 | |
 | |
| Имена | |
|---|---|
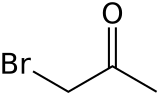
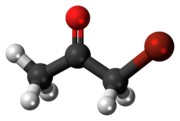
| Предпочтительное название IUPAC 1-бромопропан-2-он | |
| Другие имена Бромацетон. 1-Бром-2-пропанон. α-Бромацетон. Ацетонилбромид. Ацетилметилбромид. Бромметилметилкетон. Монобромоацетон. Мартонит. BA. UN 1569 | |
| Идентификаторы | |
| Номер CAS | |
| 3D-модель (JSmol ) | |
| ChEBI | |
| ChEMBL |
|
| ChemSpider | |
| ECHA InfoCard | 100.009.027 |
| IUPHAR / BPS | |
| PubChem CID | |
| RTECS номер |
|
| UNII | |
| CompTox Dashboard (EPA ) | |
InChI
| |
УЛЫБКИ
| |
| Свойства | |
| Химическая формула | C3H5BrO |
| Молярная масса | 136,976 г · моль |
| Внешний вид | Бесцветная жидкость |
| Плотность | 1,634 г / см |
| Температура плавления | -36,5 ° C (-33,7 ° F; 236,7 K) |
| Температура кипения | 137 ° C (279 ° F; 410 K) |
| Давление пара | 1,1 кПа (20 ° C) |
| Опасности | |
| Паспорт безопасности | MSDS в ILO |
| Температура вспышки | 51,1 ° C (124,0 ° F; 324,2 K) |
| Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки в ink | |
Бромацетон - это органическое соединение с формула C H 3CO CH2Br. Эта бесцветная жидкость является слезоточивым агентом и предшественником других органических соединений.
Бромацетон естественным образом присутствует (менее 1%) в эфирном масле морских водорослей (Asparagopsis taxiformis ) из окрестностей Гавайских островов.
Бромацетон коммерчески доступен, иногда его стабилизируют оксидом магния. Впервые он был описан в XIX веке и приписан Н. Соколовскому.
 Ацетон и бром образуют бромацетон.
Ацетон и бром образуют бромацетон. Бромацетон получают путем объединения брома и ацетона с каталитической кислота. Как и все кетоны, ацетон енолизируется в присутствии кислот или оснований. Затем альфа-углерод подвергается электрофильному замещению бромом. Основная трудность этого метода - чрезмерное бромирование, приводящее к образованию ди- и трибромированных продуктов. Если присутствует основание, вместо него получают бромоформ с помощью галоформной реакции.
. Он использовался в Первой мировой войне как химическое оружие, названное англичанами BA и немцами B-Stoff (Weisskreuz ). Из-за своей токсичности он больше не используется в качестве средства борьбы с беспорядками. Бромацетон - универсальный реагент в органическом синтезе. Это, например, предшественник гидроксиацетона в результате реакции с водным гидроксидом натрия.