| Альфред Вернер | |
|---|---|
 | |
| Родился | 12 декабря 1866 года. Мюлуз, Haut -Рин, Эльзас, Франция |
| Умер | 15 ноября 1919 (1919-11-15) (52 года). Цюрих, Швейцария |
| Национальность | Швейцар |
| Alma mater | Цюрихский университет. ETH Zurich |
| Известна | конфигурацией комплексов переходных металлов |
| Награды | Нобелевская премия по химии (1913) |
| Научная карьера | |
| Филдс | Неорганическая химия |
| Учреждения | Цюрихский университет |
| Научный руководитель | Артур Рудольф Ганцш, Марселлин Бертело |
Альфред Вернер (12 декабря 1866 - 15 ноября 1919) был швейцарским химиком, который учился в ETH Zurich и профессор Цюрихского университета. Он получил Нобелевскую премию по химии в 1913 году за предложение октаэдрической конфигурации комплексов переходных металлов. Вернер разработал основы современной координационной химии. Он был первым химиком-неоргаником, получившим Нобелевскую премию, и единственным до 1973 года.
Вернер родился в 1866 году в Мюлузе, Эльзасе (которая тогда была частью Франции, но была аннексирована Германией в 1871 году). Он был воспитан как католик. Он был четвертым и последним ребенком Жана-Адама Вернера, литейщика, и его второй жены, Саломе Жанетт Вернер, которая происходила из богатой семьи. Он отправился в Швейцарию, чтобы изучать химию в Швейцарском федеральном институте (Политехникуме) в Цюрихе, но поскольку этот институт не имел права присуждать докторские степени до 1909 года, Вернер получил докторскую степень формально в Цюрихском университете в 1890 году. После докторантуры в Париже он вернулся в Швейцарский федеральный институт, чтобы преподавать (1892). В 1893 году он перешел в Цюрихский университет, где стал профессором в 1895 году. В 1894 году он стал гражданином Швейцарии.
На последнем курсе он страдал от генерала, прогрессирующий дегенеративный атеросклероз, особенно головного мозга, усугубляемый годами чрезмерного употребления алкоголя и переутомления. Он умер в психиатрической больнице в Цюрихе.
В 1893 году Вернер первым предложил правильные структуры для координационных соединений, содержащих комплексные ионы, в котором центральный атом переходного металла окружен нейтральными или анионными лигандами.
Например, было известно, что кобальт образует «сложный» хлорид гексамминкобальта (III) с формулой CoCl 3 • 6NH 3, но природа ассоциации, обозначенной точкой, была загадочной. Вернер предложил структуру [Co (NH 3)6] Cl 3, в которой ион Co окружен шестью NH 3 в вершинах октаэдра. Три Cl диссоциируют в виде свободных ионов, что Вернер подтвердил измерением проводимости соединения в водном растворе, а также анализом хлорид-анионов с использованием осаждения нитратом серебра. Позже был проведен анализ магнитной восприимчивости также использовался для подтверждения предположения Вернера о химической природе CoCl 3 • 6NH 3.
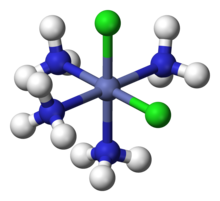 цис- [Co (NH 3)4Cl2]
цис- [Co (NH 3)4Cl2]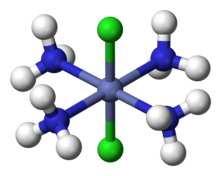 транс- [Co (NH 3)4Cl2]
транс- [Co (NH 3)4Cl2]) Для комплексов с более чем одним типом лиганда, Вернеру удалось объяснить количество наблюдаемых изомеров. Например, он объяснил существование двух изомеров тетраммина, «Co (NH 3)4Cl3», одного зеленого и одного фиолетового. Вернер предположил, что эти представляют собой два геометрических изомера формулы [Co (NH 3)4Cl2] Cl, с одним диссоциированным ионом Cl, что подтверждено измерениями проводимости. Атом Со окружен четырьмя NH 3 и двумя Cl лиганды в вершинах o f октаэдр. Зеленый изомер является «транс» с двумя лигандами Cl в противоположных вершинах, а фиолетовый - «цис» с двумя лигандами Cl в соседних вершинах.
Вернер также получил комплексы с оптическими изомерами, а в 1914 году он сообщил о первом синтетическом хиральном соединении без углерода, известном как гексол с формулой [Co (Co (NH 3)4(OH) 2)3] Br 6.
) До Вернера химики определили валентность элемента как количество его связи без различения различных типов связи. Однако в таких комплексах, как [Co (NH 3)6] Cl 3, например, Вернер считал, что связи Co-Cl соответствуют «первичной» валентности 3 на большом расстоянии, в то время как связи Co-NH 3, которые соответствуют «вторичной» или более слабой валентности 6 на более коротком расстоянии. Эту вторичную валентность 6 он назвал координационным числом которое он определил как количество молекул (здесь NH 3), непосредственно связанных с центральным атомом металла. В других комплексах он обнаружил координационные числа 4 или 8.
На основании этих взглядов, и другие подобные взгляды, в 1904 г. Ричард Абегг сформулировал t теперь известно как правило Абегга, которое гласит, что разница между максимальной положительной и отрицательной валентностью элемента элемента часто равна восьми. Это правило было использовано позже, в 1916 году, когда Гилберт Н. Льюис сформулировал «правило октетов » в своей теории кубического атома.
В современной терминологии первичная валентность Вернера соответствует степени окисления, а его вторичная валентность называется координационным числом. Связи Co-Cl (в приведенном выше примере) теперь классифицируются как ионные, и каждая связь Co-N представляет собой координационную ковалентную связь между кислотой Льюиса Co и База Льюиса NH3.