Деградация Вермана, также называемая реакция Вермана, является именной реакцией по органической химии. Он назван в честь того, кто открыл его в 1910 году. В общем, это органическая реакция в химии углеводов, в которой амиды разлагаются гипохлоритом натрия, образуя альдегид с одним атомом углерода меньше. Некоторые рассматривают это как продолжение перегруппировки Хофмана.
Разложение Верманна может быть выполнено с помощью α-гидроксизамещенных амидов угольной кислоты. Например, сахар.
Во время разложения α-гидроксизамещенных амидов угольной кислоты углеродная цепь укорачивается на один атом углерода.

Реакция протекает очень медленно. при комнатной температуре, поэтому реакционная смесь нагревается до 60-65 °C.
Механизм реакции является механизмом связанной деградации Гофмана.

Сначала амид угольной кислоты (1) реагирует с гипохлоритом натрия. После разделения воды и хлорида образуется амин со свободной связью 2 . Промежуточное звено (3) генерируется перегруппировкой. На следующем этапе происходит гидролиз. Вода добавляется у атома углерода с номером «1» . Образуется гидроксильная группа. Последней стадией является отделение кислого амида и образование альдегида (4) .
Кроме того, деградация Вермана может быть осуществлена с помощью α, β-ненасыщенных амидов угольной кислоты. Например, акриламид.
Во время разложения α-гидроксизамещенных амидов угольной кислоты углеродная цепь также укорачивается примерно на один атом углерода.

Реакция протекает очень медленно при комнатной температуре, поэтому реакционная смесь нагревается до 60–65 °C.
Механизм реакции является механизмом связанной деградации Гофмана.

При сначала амид угольной кислоты (1) реагирует с гипохлоритом натрия. После разделения воды и хлорида образуется амин со свободной связью 2 . Промежуточное звено (3) генерируется перегруппировкой. На этом этапе возможны два разных механизма. В указанном выше механизме две молекулы метанола реагируют с промежуточным продуктом. Так создается соединение (4) . После этого диоксид углерода, вода, аммоний и метанол разделяются на разных этапах. По крайней мере, он протонирован в альдегид (5) .
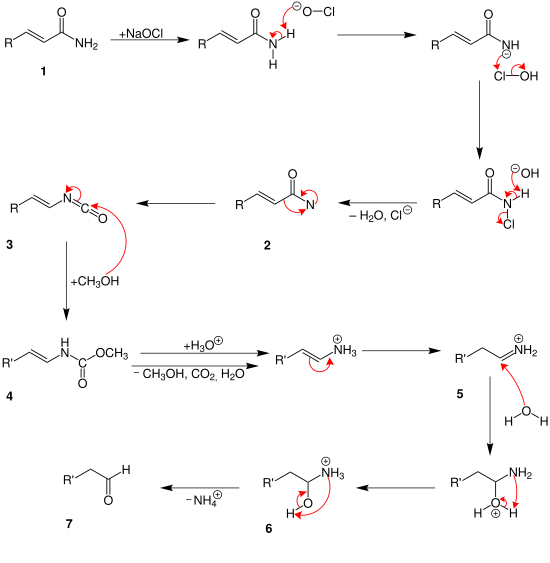
. До промежуточного соединения (3) механизм такой же, как указано выше. Затем добавляется только один атом метанола 4 . С помощью протонирующей воды разделяют метанол и диоксид углерода. Образуется ион аммония (5) . Во время гидролиза образуется гидроксильная группа 6 . Альдегид (7) образуется путем отделения иона аммония.
Одно исследование продемонстрировало прямое окисление глюкозы до арабинозы тем же гипохлоритом натрия, пропуская стадии альдоновой кислоты и альдоамида. Например, общее разложение D-глюконамида до D-арабинозы:

Кроме того, можно использовать тест Вермана, чтобы показать, находится ли гидроксильная группа рядом с амидогруппой. Эта реакция важна только в историческом смысле, потому что она медленно поддается и поэтому редко используется.