 | |
 | |
| Имена | |
|---|---|
| IUPAC имя три-μ-карбонил-1: 2κC; 1: 3κC; 2: 3κC-нонакарбонил- 1κC, 2κC, 3κC, 4κC- [T d - (13) -Δ -клозо] - тетрародий (6 Rh-Rh) | |
| Другие названия родий (0) карбонил; карбонил родия; додекакарбонил родия | |
| Идентификаторы | |
| Номер CAS | |
| 3D-модель (JSmol ) | |
| ECHA InfoCard | 100.039.232 |
| Панель инструментов CompTox (EPA ) | |
УЛЫБКИ
| |
| Свойства | |
| Химическая формула | Rh4(CO) 12 |
| Молярная масса | 747,743 г / моль |
| Внешний вид | Красные кристаллы |
| Растворимость | Хлороуглероды, толуол, тетрагидрофуран |
| Родственные соединения | |
| Родственные соединения | хлорид родия (III), Rh 6 (CO) 16, Rh 2 (CO) 4Cl2 |
| Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки в ink | |
Тетрародий додекакарбонил - это химическое соединение с формулой Rh4(CO) 12. Это темно-красное кристаллическое твердое вещество является самым маленьким стабильным двойным роди гм карбонил. Он используется в качестве катализатора в органическом синтезе.
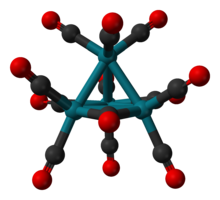
Структура Rh 4 (CO) 12 описывается тетраэдрическим массивом из четырех атомов Rh с девятью концевыми CO лиганды и три мостиковых CO-лиганда. Структура может быть выражена как Rh 4 (CO) 9 (µ-CO) 3. Его получают обработкой водного раствора трихлорида родия активированным металлом медь в атмосфере CO.
Альтернативно, соединение может быть получено обработкой метанольный раствор RhCl 3(H2O)3 с CO с получением H [RhCl 2 (CO) 2 ] с последующим карбонилированием в присутствии цитрат натрия.
Кластер подвергается термическому замещению фосфорными лигандами, L:
Из-за их значимости для катализа гидроформилирования, карбонилы металлов имеют систематически изучены в высокой степени. Нестабильность Rh 2 (CO) 8 вызвала любопытство. Аналогичный бинарный карбонил кобальта, Co2(CO) 8, хорошо известен. Растворы Rh 4 (CO) 12 при высоком давлении CO превращаются в соединение диродия:
В отличие от Co 2 (CO) 8, который содержит мостиковые карбонилы, основной изомер Rh 2 ( CO) 8 содержит только концевые лиганды CO. Относительная нестабильность Rh 2 (CO) 8 аналогична тенденции Ru (CO) 5 преобразовываться в Ru 3 ( CO) 12.