 | |
| Имена | |
|---|---|
| Название IUPAC Монохлорид селена | |
| Другие названия Дихлородиселенид, дихлорид дизелена, хлорид селена, 1,2-дихлордиселан | |
| Идентификаторы | |
| Номер CAS | |
| 3D-модель (JSmol ) | |
| ChemSpider | |
| ECHA InfoCard | 100.030.022 |
| PubChem CID | |
| UNII | |
| Панель управления CompTox (EPA ) | |
InChI
| |
SMILES
| |
| Свойства | |
| Химическая формула | Se2Cl2 |
| Молярная масса | 228,83 г / моль |
| Внешний вид | Красновато-коричневая маслянистая жидкость |
| Плотность | 2,7741 г / см |
| Расплав точка входа | -85 ° C (-121 ° F; 188 K) |
| Температура кипения | 127 ° C (261 ° F; 400 K) при 0,997 атм |
| Растворимость в воде | нерастворим |
| Растворимость в других растворителях | Растворим в хлороформе, сероуглероде и ацетонитриле |
| Магнитная восприимчивость (χ) | -94,8 · 10 см / моль |
| Опасности | |
| R-фразы (устарело) | R23 / 24/25 -R34 |
| S-фразы (устаревшие) | S22 -S26 -S36 / 37/39 -S45 |
| Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобокс | |
Монохлорид селена представляет собой неорганическое соединение с формулой Se 2Cl2. Хотя его называют монохлоридом селена, более описательным названием может быть дихлорид диселена. Это красновато-коричневая маслянистая жидкость, которая медленно гидролизуется. Он существует в химическом равновесии с SeCl 2, SeCl 4, хлором и элементарным селеном. Монохлорид селена в основном используется в качестве реагента для синтеза Se-содержащих соединений.
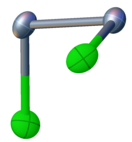
Монохлорид селена связан с Cl-Se-Se-Cl. Обладая неплоской структурой, он имеет симметрию молекулы C 2, аналогичную пероксиду водорода и монохлориду серы. Длина связи Se-Se составляет 2,23 Å, а длина связи Se-Cl составляет 2,20 Å. Двугранный угол составляет 87 °.
Монохлорид селена первоначально получали хлорированием селена. Усовершенствованный метод включает реакцию смеси селена, диоксида селена и соляной кислоты:
Плотный слой монохлорида селена осаждается из реакционной смеси, которую можно очистить путем растворения его в дымящей серной кислоте и повторного осаждения с помощью соляной кислоты. Второй метод синтеза включает реакцию селена с олеумом и соляной кислотой:
Неочищенный монохлорид селена собирают перегонкой.
В растворах ацетонитрила он находится в равновесии с SeCl 2 и SeCl 4.Дихлорид селена разлагается до монохлорида через несколько минут при комнатной температуре. :
Монохлорид селена является электрофильным селенизирующим агентом и, таким образом, реагирует с простыми алкенами чтобы получить бис (β-хлоралкил) селенид и бис (хлоралкил) дихлорид селена. Он превращает гидразоны затрудненных кетонов в соответствующие селенокетоны, структурные аналоги кетонов, в которых атом кислорода заменяется атомом селена. Наконец, соединение было использовано для введения мостиковых селеновых лигандов между атомами металлов некоторых карбонильных комплексов железа и хрома.