The SCNN1G ген кодирует субъединицу γ эпителиального натриевого канала ENaC у позвоночных. ENaC собирается как гетеротример, состоящий из трех гомологичных субъединиц α, β и γ или δ, β и γ. Другие субъединицы ENAC кодируются SCNN1A, SCNN1B и SCNN1D.
ENaC экспрессируется в эпителиальных клетках и отличается от потенциалзависимого натриевого канала, который участвует в генерации потенциалов действия в нейронах. Аббревиатура генов, кодирующих потенциал-управляемые натриевые каналы, начинается с трех букв: SCN. В отличие от этих натриевых каналов, ENaC конститутивно активен и не зависит от напряжения. Вторая буква N в аббревиатуре (SCNN1) означает, что это каналы, НЕ управляемые напряжением.
У большинства позвоночных ионы натрия являются основным фактором, определяющим осмолярность внеклеточной жидкости. ENaC позволяет переносить ионы натрия через мембрану эпителиальных клеток в так называемом «плотном эпителии», который имеет низкую проницаемость. Поток ионов натрия через эпителий влияет на осмолярность внеклеточной жидкости. Таким образом, ENaC играет центральную роль в регуляции гомеостаза жидкости и электролитов в организме и, следовательно, влияет на кровяное давление.
Поскольку ENaC сильно ингибируется амилоридом, его также называют « амилорид-чувствительный натриевый канал ».
первая кДНК, кодирующая гамма-субъединицу ENaC, была клонирована и секвенирована Canessa et al. из мРНК крысы. Год спустя две независимые группы сообщили о последовательностях кДНК бета- и гамма-субъединиц человеческого ENaC. Полная кодирующая последовательность γ-субъединицы человека была описана Saxena et al.
В то время как человеческий ген SCNN1A расположен в хромосоме 12p, человеческие гены, кодирующие SCNN1B и SCNN1G расположены в juxtoposition в коротком плече хромосомы 16 (16p12-p13). О структурах генов SCNN1G человека и крысы впервые сообщили Thomas et al. Более поздние исследования Saxena et al. сообщили о полной кодирующей последовательности гена SCNN1G человека, установив, что он имеет 13 экзонов. Положения интронов консервативны во всех трех генах ENaC человека, SCNN1A, SCNN1B и SCNN1G. Положения интронов также высоко консервативны у позвоночных. См. Ensembl GeneTree.
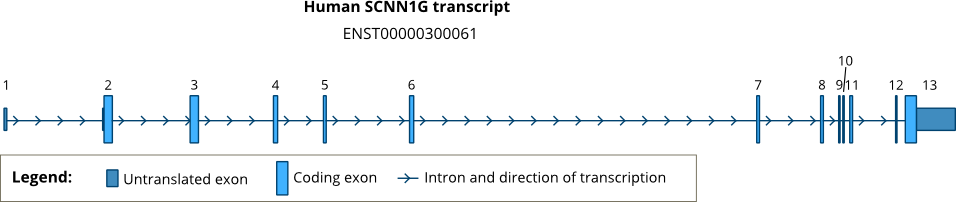 Рис. 1. Экзон-интронная структура основного транскрипта человеческого SCNN1B. Номер каждого экзона отмечен над экзоном. Серийный номер стенограммы указан над ней. Щелчок по рисунку направит читателя к списку транскриптов в базе данных Ensembl.
Рис. 1. Экзон-интронная структура основного транскрипта человеческого SCNN1B. Номер каждого экзона отмечен над экзоном. Серийный номер стенограммы указан над ней. Щелчок по рисунку направит читателя к списку транскриптов в базе данных Ensembl. Три субъединицы ENaC, кодируемые SCNN1A, SCNN1B и SCNN1G, являются обычно выражается в плотном эпителии с низкой водопроницаемостью. Основные органы, в которых экспрессируется ENaC, включают части эпителия почечных канальцев, дыхательные пути, женские половые пути, толстую кишку, слюнные и потовые железы.
ENaC также экспрессируется на языке, где это было показано. имеет важное значение для восприятия соленого вкуса.
Экспрессия генов субъединиц ENaC регулируется в основном минералокортикоидным гормоном альдостероном, который активируется ренин-ангиотензиновой системой.
Первичные структуры всех четырех субъединиц ENaC демонстрируют сильное сходство. Таким образом, эти четыре белка представляют собой семейство белков, имеющих общего предка. При глобальном выравнивании (то есть выравнивании последовательностей по всей их длине, а не только частичном сегменте) субъединица γ человека имеет 34% идентичности с субъединицей β и 27 и 23% идентичности с субъединицами α и δ.
Все четыре последовательности субъединиц ENaC имеют два гидрофобных участка, которые образуют два трансмембранных сегмента, названных TM1 и TM2. В мембраносвязанной форме сегменты TM встроены в бислой мембраны, амино- и карбоксиконцевые области расположены внутри клетки, а сегмент между двумя TM остается вне клетки в качестве внеклеточной области ENaC. Эта внеклеточная область включает около 70% остатков каждой субъединицы. Таким образом, в мембраносвязанной форме основная часть каждой субъединицы находится вне клетки.
Структура ENaC еще не определена. Тем не менее, структура гомологичного белка ASIC1 была определена. Структура ASIC1 курицы выявила, что ASIC1 собран как гомотример из трех идентичных субъединиц. Авторы оригинального исследования предположили, что тример ASIC1 напоминает руку, держащую мяч. Следовательно, отдельные домены ASIC1 были названы ладонью, суставом, пальцем, большим пальцем и β-шариком.
Сайт-направленный мутагенез субъединицы γ человека предполагает, что субъединицы ENaC имеют структуру, аналогичную структуре ASIC1.. Фильтр ионной селективности ENaC был смоделирован на основе структуры ASIC1.
Выравнивание последовательностей субъединиц ENaC с последовательностью ASIC1 показывает, что сегменты TM1 и TM2 и домен ладони сохранены, а домены суставов, пальцев и большого пальца имеют прошивки в ENaC. Исследования сайт-направленного мутагенеза субъединиц ENaC предоставляют доказательства того, что многие основные особенности структурной модели ASIC1 применимы и к ENaC.
На карбоксильном конце трех субъединиц ENaC (α, β и γ) имеется специальная консервативная консенсусная последовательность PPPXYXXL, которая называется мотивом PY. Эта последовательность распознается так называемыми WW-доменами в специальной убиквитин-протеинлигазе E3, названной Nedd4-2. Nedd4-2 лигирует убиквитин с С-концом субъединицы ENaC, который отмечает расщепление белка.
В настоящее время известны три основных наследственных заболевания быть связанным с мутациями в гене SCNN1G. К ним относятся: 1. Мультисистемный псевдогипоальдостеронизм, 2. Синдром Лиддла и 3. Заболевание, подобное муковисцидозу.
Заболевание, которое чаще всего ассоциируется с мутациями в SCNN1B - мультисистемная форма псевдогипоальдостеронизма I типа (PHA1B), которая была впервые охарактеризована А. Ханукоглу как аутосомно-рецессивное заболевание. Это синдром невосприимчивости к альдостерону у пациентов с высоким уровнем альдостерона в сыворотке крови, но страдающих от симптомов дефицита альдостерона с высоким риском смерти из-за тяжелой потери соли. Первоначально считалось, что это заболевание является результатом мутации рецептора минералокортикоидов (NR3C2), который связывает альдостерон. Но картирование гомозиготности в 11 затронутых семьях показало, что заболевание связано с двумя локусами на хромосоме 12p13.1-pter и хромосоме 16p12.2-13, которые включают гены SCNN1A, SCNN1B и SCNN1G соответственно. Секвенирование генов ENaC выявило мутации у пораженных пациентов, а функциональная экспрессия мутированных кДНК дополнительно подтвердила, что выявленные мутации приводят к потере активности ENaC.
У большинства пациентов с мультисистемным PHA1B a Обнаружена гомозиготная мутация или две сложные гетерозиготные мутации.
Синдром Лиддла обычно вызывается мутациями в мотиве PY или усечением С-конца, включая потерю мотива PY в субъединицы β или γ ENaC. Даже несмотря на то, что мотив PY присутствует также в α-субъединице, до сих пор болезнь Лиддла не наблюдалась в связи с мутацией в α-субъединице. Синдром Лиддла наследуется как аутосомно-доминантное заболевание с фенотипом, который включает гипертензию с ранним началом, метаболический алкалоз и низкие уровни активности ренина в плазме и альдостерона минералокортикоидного гормона. В отсутствие узнаваемого мотива PY убиквитин-протеинлигаза Nedd4-2 не может связываться с субъединицей ENaC и, следовательно, не может присоединять к ней убиквитин. Следовательно, протеолиз ENaC протеасомой ингибируется, и ENaC накапливается в мембране, что приводит к усилению активности ENaC, вызывающей гипертензию.
Было показано, что SCNN1G взаимодействует с: