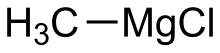 | |
| Имена | |
|---|---|
| Название ИЮПАК хлоридо (метил) магний | |
| Другие названия (хлормагнезио) метан | |
| Идентификаторы | |
| Количество CAS | |
| 3D модель ( JSmol ) | |
| ЧЭБИ | |
| ChemSpider | |
| ECHA InfoCard | 100.010.573 |
| PubChem CID | |
| UNII | |
| Панель управления CompTox ( EPA) | |
ИнЧИ
| |
Улыбки
| |
| Характеристики | |
| Химическая формула | CH 3 MgCl |
| Молярная масса | 74,79 г / моль |
| Появление | бесцветное твердое вещество |
| Растворимость в воде | Реагирует с водой |
| Растворимость | растворим в диэтиловом эфире и ТГФ |
| Опасности | |
| Основные опасности | Легковоспламеняющийся, Реагирует с водой |
| NFPA 704 (огненный алмаз) |  3 3 2 3 3 2 |
| точка возгорания | -17 ° С |
| Родственные соединения | |
| Родственные соединения | Бромид фенилмагния, дибутилмагний |
| Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |
| | |
| Ссылки на инфобоксы | |
Хлорид метилмагния представляет собой металлоорганическое соединение с общей формулой CH 3 MgCl. Этот легковоспламеняющийся, бесцветный и чувствительный к влаге материал является простейшим реактивом Гриньяра и коммерчески доступен, обычно в виде раствора в тетрагидрофуране.
По сравнению с более часто встречающимися метилмагнийбромидом и метилмагниййодидом, метилмагнийхлорид обладает такими преимуществами, как низкий эквивалентный вес и низкая стоимость. Его получают реакцией хлористого метила и магния в этиловом эфире.
 Структура CH 3 MgCl (thf) 2, которая является представителем разновидностей в донорных растворителях.
Структура CH 3 MgCl (thf) 2, которая является представителем разновидностей в донорных растворителях. Как и большинство реактивов Гриньяра, метилмагнийхлорид сильно сольватируется эфирными растворителями за счет координации двух атомов кислорода с образованием тетраэдрически связанного магниевого центра.
Как метиллития, это синтетический эквивалентно метил карбанион синтона. Он реагирует с водой и другими протонными реагентами с образованием метана, например:
При обработке диоксаном хлорид метилмагния превращается в диметилмагний через равновесие Шленка :