 | |
| Идентификаторы | |
|---|---|
| Номер CAS | |
| 3D-модель (JSmol ) | |
| ChemSpider | |
| MeSH | гем + C |
| PubChem CID | |
InChI
| |
УЛЫБАЕТСЯ
| |
| Свойства | |
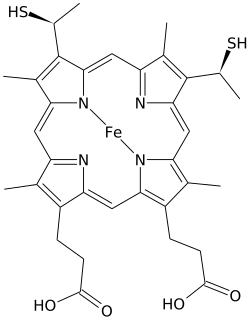
| Химическая формула | C34H36O4N4S2Fe |
| Молярная масса | 684,64904 г / моль |
| Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки в инфобоксе | |
Гем C (или гем C ) - важный вид гема.
Правильная структура гема C была опубликована в середине 20 века шведским биохимиком К.-Г. Павел. Эта работа подтвердила структуру, впервые предложенную великим шведским биохимиком Хьюго Теоретлом. Структура гема C, основанная на экспериментах ЯМР и ИК восстановленной, Fe (II), формы гема, была подтверждена в 1975 году. Структура гема C, включая абсолютную стереохимическую конфигурацию относительно тиоэфира. Связи были впервые представлены для белка позвоночных, цитохрома c, а теперь распространены на многие другие белки, содержащие гем C.
Гем C отличается от гема B тем, что две винил боковые цепи гема B заменены ковалентным, тиоэфиром. связан с апопротеином. Две тиоэфирные связи обычно образуются остатками цистеина в белке. Эти связи не позволяют гему С легко диссоциировать от голопротеина, цитохрома с по сравнению с более легко диссоциированным гемом В, который может диссоциировать от голопротеина, комплекса гем-белок., даже в мягких условиях. Это позволяет использовать очень широкий диапазон структуры и функций цитохрома c, при этом мириады цитохромов типа c действуют в основном как переносчики электронов. Окислительно-восстановительный потенциал цитохрома с можно также «настроить» небольшими изменениями в структуре белка и взаимодействии с растворителем.
Количество единиц гема C, связанных с голопротеином, сильно варьируется. Для клеток позвоночных один гем С на белок является правилом, но для бактерий это количество часто составляет 2, 4, 5, 6 или даже 16 гемовых групп С на голопротеин. Принято считать, что количество и расположение групп гема С связаны и даже необходимы для правильной функции голопротеина. Например, белки, содержащие несколько групп гема C, участвуют во множественных реакциях переноса электронов, особенно важным является восстановление на 6 электронов, необходимое для восстановления атмосферного азота до двух органических молекул аммиака. Для бактериальных гемепротеинов отношение гема С к аминокислоте является обычным, поэтому внутренняя часть некоторых белков цитохрома с кажется заполненной многими группами гема С по сравнению с другими гемепротеинами. Некоторые гемепротеины, часто получаемые из одноклеточных организмов, могут содержать пять гемов C. bc1Комплекс является еще одним важным ферментом, который содержит гем типа C.
Тиоэфирные связи, по-видимому, предоставляют большую свободу функций голопротеинам. В общем, цитохромы c-типа можно «точно настроить» в более широком диапазоне окислительно-восстановительного потенциала, чем цитохромы b. Это может быть важной причиной того, что цитохром с почти повсеместен на протяжении всей жизни. Гем C также играет важную роль в апоптозе, когда всего несколько молекул цитоплазматического цитохрома c, которые все еще должны содержать гем C, приводят к запрограммированной гибели клеток. Цитохром c может быть измерен в сыворотке крови человека и может использоваться в качестве маркера воспаления.
В дополнение к этим экваториальным ковалентным связям гемовое железо также обычно аксиально скоординировано с боковыми цепями двух амино кислоты, делая гексакоординированное железо. Например, у млекопитающих и тунца цитохром с содержат один гем С, который аксиально скоординирован с боковыми цепями как гистидина, так и метионина. Возможно, из-за двух ковалентных связей, удерживающих гем с белком, железо гема С иногда аксиально лигируется с аминогруппой лизина или даже с водой.