Кальсеквестрин
редактировать
Кальсеквестрин представляет собой кальций-связывающий белок, который действует как кальциевый буфер в саркоплазматическом ретикулум. Белок помогает удерживать кальций в цистерне саркоплазматического ретикулума после мышечного сокращения, даже несмотря на то, что концентрация кальция в саркоплазматическом ретикулуме намного выше, чем в цитозоле. Это также помогает саркоплазматическому ретикулуму накапливать чрезвычайно большое количество ионов кальция. Каждая молекула кальсеквестрина может связывать от 18 до 50 ионов Са. Анализ последовательности показал, что кальций связывается не в отдельных карманах через мотивы EF-hand, а скорее через представление заряженного белка поверхность. Были идентифицированы две формы кальсеквестрина. Кардиальная форма кальсеквестрина-2 (CASQ2) присутствует в сердечных и медленных скелетных мышцах, а быстрая скелетная форма кальсеквестрин-1 (CASQ1) обнаруживается в быстрых скелетных мышцах. Высвобождение кальция, связанного с кальсеквестрином (через канал высвобождения кальция), вызывает сокращение мышц. Активный белок не очень структурирован, более 50% его принимает конформацию случайного клубка. Когда кальций связывается, происходит структурное изменение, в результате чего содержание альфа-спирали белка увеличивается с 3 до 11%. Обе формы кальсеквестрина фосфорилируются с помощью казеинкиназы 2, но сердечная форма фосфорилируется быстрее и в большей степени. Кальсеквестрин также секретируется в кишечнике, где он лишает бактерии ионов кальция.
Содержание
- 1 Сердечный кальсеквестрин
- 2 См. Также
- 3 Ссылки
- 4 Дополнительная литература
- 5 Внешние ссылки
Кардиальный кальсеквестрин
Кардиальный кальсеквестрин (CASQ2) играет важную роль в регуляции сердечной деятельности. Мутации в сердечном гене кальсеквестрина были связаны с сердечной аритмией и внезапной смертью. Считается, что CASQ2 играет роль в регулировании сердечной связи возбуждения и сокращения и кальциевого высвобождения кальция (CICR) в сердце, поскольку избыточная экспрессия CASQ2, как было показано, существенно увеличивает величина усредненных по клеткам I CA переходных процессов кальция и спонтанных кальциевых искр в изолированных клетках сердца. Кроме того, CASQ2 модулирует механизм CICR, удлиняясь до процесса, чтобы функционально перезарядить запасы ионов кальция в саркоплазматическом ретикулуме. Отсутствие или мутация CSQ2 напрямую связаны с катехоламинергической полиморфной желудочковой тахикардией (CPVT). Мутация может иметь значительный эффект, если нарушает способность CASQ2 к линейной полимеризации, что напрямую объясняет его высокую способность связывать Ca. Кроме того, гидрофобное ядро домена II, по-видимому, необходимо для функции CASQ2, потому что мутация одной аминокислоты, которая разрушает это гидрофобное ядро, напрямую приводит к молекулярным агрегатам, которые не могут реагировать на ионы кальция.
См. также
Ссылки
Дополнительная литература
- Wang S, Trumble WR, Liao H, Wesson CR, Dunker AK, Kang CH (1998). «Кристаллическая структура кальсеквестрина из саркоплазматического ретикулума скелетных мышц кролика». Nat. Struct. Биол. 5 (6): 476–83. doi : 10.1038 / nsb0698-476. PMID 9628486. S2CID 7967757.
Внешние ссылки
Эта статья включает текст из общественного достояния
Pfam и
InterPro :
IPR001393 .
 мономер кальсеквестрина с тремя повторяющимися доменами кальсеквестрина
мономер кальсеквестрина с тремя повторяющимися доменами кальсеквестрина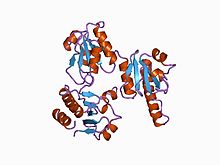 Кристаллическая структура кальсеквестрина из саркоплазматического ретикулума скелетных мышц кролика при разрешении 2,4
Кристаллическая структура кальсеквестрина из саркоплазматического ретикулума скелетных мышц кролика при разрешении 2,4