 Мономерный, левосторонний β- helix антифриз белка еловой почковой червя Choristoneura fumiferana (PDB : 1M8N ).
Мономерный, левосторонний β- helix антифриз белка еловой почковой червя Choristoneura fumiferana (PDB : 1M8N ). 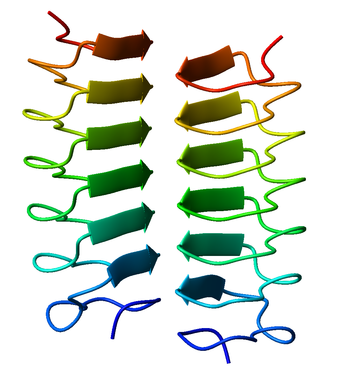 Димерный правосторонний антифриз β-спиральный белок жука Tenebrio molitor (PDB : 1EZG ). Прямая ассоциация β-спиралей.
Димерный правосторонний антифриз β-спиральный белок жука Tenebrio molitor (PDB : 1EZG ). Прямая ассоциация β-спиралей. A бета-спираль представляет собой структуру тандемного повтора белка, образованную объединением параллельных бета-цепей в спиральном узоре с либо два, либо три лица. Бета-спираль представляет собой тип соленоидного белкового домена. Структура стабилизирована межцепочечными водородными связями, белок-белковыми взаимодействиями и иногда связанными ионами металлов . Идентифицированы как левая, так и правая бета-спирали. Двухцепочечные бета-спирали также являются очень распространенными характеристиками белков и обычно являются синонимами складок желеобразного валика.
. Первая бета-спираль наблюдалась в ферменте пектатлиазе, который содержит семи- спираль поворота достигает 34 Å (3,4 нм ) в длину. Хвостовой белок фага P22, компонент бактериофага P22 , имеет 13 витков, а длина собранного гомо тример составляет 200 Å (20 нм).. Его внутренняя часть плотно упакована без центральной поры и содержит как гидрофобные остатки, так и заряженные остатки, нейтрализованные солевыми мостиками.
И пектатлиаза, и белок хвостовой спинки P22 содержат правые спирали; левосторонние версии наблюдались в ферментах, таких как архейная карбоангидраза. Другие белки, которые содержат бета-спирали, включают белки антифриза жука Tenebrio molitor (правосторонний) и елового почкопряда Choristoneura fumiferana (левосторонний), где регулярно расположенные треонины на β-спиралях связываются с поверхностью кристаллов льда и ингибируют их рост.
Бета-спирали могут эффективно связываться друг с другом, либо лицом к лицу (сопрягая грани своих треугольных призм), либо встык (образуя водородные связи). Следовательно, β-спирали можно использовать в качестве «меток» для побуждения других белков к ассоциации, подобно сегментам спиральной спирали.
Было показано, что члены семейства пентапептидных повторов обладают четырехугольной бета-спиральной структурой.