| Альфа-глюкозидаза | |||||||||
|---|---|---|---|---|---|---|---|---|---|
| Идентификаторы | |||||||||
| ЕС нет. | 3.2.1.20 | ||||||||
| № CAS | 9001-42-7 | ||||||||
| Базы данных | |||||||||
| IntEnz | Просмотр IntEnz | ||||||||
| BRENDA | BRENDA запись | ||||||||
| ExPASy | Просмотр NiceZyme | ||||||||
| КЕГГ | Запись в KEGG | ||||||||
| MetaCyc | метаболический путь | ||||||||
| ПРИАМ | профиль | ||||||||
| Структуры PDB | RCSB PDB PDBe PDBsum | ||||||||
| |||||||||
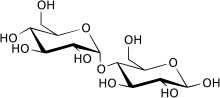 Мальтоза
Мальтоза  Взаимодействие лиганда (NAG) в мальтазе-глюкоамилазе
Взаимодействие лиганда (NAG) в мальтазе-глюкоамилазе  Взаимодействие олигосахаридов в альфа-амилазе
Взаимодействие олигосахаридов в альфа-амилазе Мальтаза ( EC 3.2.1.20, альфа-глюкозидаза, глюкоинвертаза, глюкозидосахараза, мальтаза-глюкоамилаза, альфа-глюкопиранозидаза, глюкозидоинвертаза, альфа-D-глюкозидаза, альфа-глюкозидгидролаза, альфа-1,4-глюкозидаза, альфа-D-глюкозид глюкогидролаза) представляет собой один из типов ферментов альфа-глюкозидазы, расположенных в щеточной кайме тонкой кишки. Этот фермент катализирует гидролиз дисахарида мальтозы до двух простых сахаров глюкозы.. Мальтаза содержится в растениях, бактериях, дрожжах, людях и других позвоночных. Считается, что он синтезируется клетками слизистой оболочки, выстилающей стенку кишечника.
Для переваривания крахмала требуется шесть кишечных ферментов. Два из этих ферментов представляют собой люминальные эндоглюкозидазы, называемые альфа-амилазами. Остальные четыре фермента были идентифицированы как разные мальтазы, экзоглюкозидазы, связанные с люминальной поверхностью энтероцитов. Две из этих мальтазных активностей были связаны с сахарозой-изомальтазой (мальтаза Ib, мальтаза Ia). Две другие мальтазы без каких-либо отличительных характеристик были названы мальтаза-глюкоамилаза (мальтазы II и III). Активность этих четырех мальтаз также описывается как альфа-глюкозидаза, потому что все они расщепляют линейные олигосахариды крахмала до глюкозы.
В большинстве случаев он эквивалентен альфа-глюкозидазе, но термин «мальтаза» подчеркивает дисахаридную природу субстрата, от которого отщепляется глюкоза, а «альфа-глюкозидаза» подчеркивает связь, независимо от того, является ли субстрат дисахаридом или полисахаридом.
Летучие мыши-вампиры - единственные позвоночные, которые, как известно, не проявляют активности кишечной мальтазы.
Мальтаза является частью группы кишечных ферментов под названием FamilyGH13 ( семейство гликозидгидролаз 13 ), которые отвечают за разрушение α-глюкозидазных связей сложных углеводов на простые в использовании молекулы глюкозы. Затем молекулы глюкозы будут использоваться как своего рода «пища» для клеток, чтобы производить энергию ( аденозинтрифосфат ) во время клеточного дыхания. Следующие гены могут кодировать мальтазу:
 Реакция гидролиза мальтозы нарушается по 1-4 альфа-глюкозидазной связи.
Реакция гидролиза мальтозы нарушается по 1-4 альфа-глюкозидазной связи. Механизм всех ферментов FamilyGH13 заключается в разрыве связи α-глюкозидазы путем ее гидролиза. Мальтаза фокусируется на расщеплении мальтозы, дисахарида, который является связующим звеном между 2 единицами глюкозы по связи α- (1-gt; 4). Скорость гидролиза контролируется размером субстрата (размером углеводов).
Альфа-амилаза играет важную роль в разложении крахмалов, поэтому ее очень часто используют в хлебопекарной промышленности. В основном он используется для улучшения вкуса хлеба. Без альфа-амилазы дрожжи не могли бы ферментировать.
Мальтозоглюкоамилаза обычно используется в качестве источника ферментации, поскольку она способна превращать крахмал в мальтозу, которая затем используется для пивоварения и саке.
Помимо пивоварения, мальтозоглюкоамилаза изучалась путем введения специфических ингибиторов, останавливающих гидролиз α-глюкозидазных связей. Подавляя разрыв связей, ученые надеются разработать лекарство, которое будет более эффективным и менее токсичным для лечения диабета.
История открытия мальтазы началась, когда Наполеон Бонапарт объявил континентальную блокаду своим «Берлинским указом» в 1806 году. Это положило начало поиску альтернативных источников сахара. В 1833 году французские химики Ансельм Пайен и Жан-Франсуа Персо открыли солодовый экстракт, который превращал крахмал в глюкозу, которую они в то время называли диастазой. В 1880 году Х.Т. Браун обнаружил активность мальтазы слизистых оболочек и дифференцировал ее от диастазы, которая теперь называется амилазой. В 1960-х годах достижения в области химии белков позволили Арне Дальквисту и Джорджио Семенце фракционировать и охарактеризовать активность мальтазы тонкого кишечника. Обе группы показали наличие четырех основных фракций мальтазной активности, присущих двум различным пептидным структурам, сахарозе-изомальтазе и мальтаза-глюкоамилазе. Пятьдесят лет спустя, вступив в эпоху генома, клонирование и секвенирование гидролазы крахмала слизистой оболочки подтвердили открытия Дальквиста и Семензы.
Дефицит кислотной мальтазы (AMD), также известный как болезнь Помпе, был впервые описан голландским патологом JC Pompe в 1932 году. AMD - это аутосомно-рецессивное заболевание, не связанное с полом, при котором чрезмерное накопление гликогена накапливается в вакуолях лизосом почти во всех типах клеток повсюду. тело. Это одно из наиболее серьезных заболеваний, связанных с накоплением гликогена, поражающих мышечную ткань.
AMD подразделяется на три отдельных типа в зависимости от возраста появления симптомов у пораженного человека. Инфантильность (Тип а), детство (Тип b) и взросление (Тип c). Тип AMD определяется типом мутации гена, локализованной на 17q23. Тип мутации определяет уровень продукции кислой мальтазы. AMD чрезвычайно смертельна. Типа обычно умирают от сердечной недостаточности в возрасте до одного года. Тип b умирает от дыхательной недостаточности в возрасте от трех до двадцати четырех лет. Тип c умирает от дыхательной недостаточности через 10-20 лет после появления симптомов.