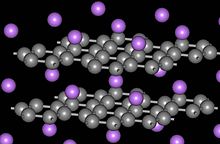
 (вид сбоку)
(вид сбоку)  (вид сверху) Модель заполнения пространства калиевого графита KC 8.
(вид сверху) Модель заполнения пространства калиевого графита KC 8.Графит соединения интеркаляции (GIC ) представляют собой сложные материалы, имеющие формулу CX m, где ион X или X вставлен (интеркалирован ) между противоположно заряженным углеродом слои. Обычно m намного меньше 1. Эти материалы представляют собой твердые твердые вещества с глубоким окрашиванием, которые обладают рядом электрических и окислительно-восстановительных свойств для потенциальных применений.
Эти материалы получают обработкой графита сильным окислителем или сильным восстановителем:
Реакция обратима.
Хост (графит) и гость X взаимодействуют посредством передачи заряда. Аналогичный процесс лежит в основе коммерческих литий-ионных аккумуляторов.
В смеси с интеркаляцией графита не каждый слой обязательно занят гостями. В так называемых соединениях стадии 1 графитовые слои и интеркалированные слои чередуются, а в соединениях стадии 2 два графитовых слоя без промежуточного материала чередуются с интеркалированным слоем. Фактический состав может варьироваться, и поэтому эти соединения являются примером нестехиометрических соединений. Принято указывать композицию вместе со сценой. Слои раздвигаются при включении гостевых ионов.
 Калиевый графит в атмосфере аргона в колбе Шленка. Также присутствует покрытая стеклом магнитная мешалка.
Калиевый графит в атмосфере аргона в колбе Шленка. Также присутствует покрытая стеклом магнитная мешалка. Одно из наиболее изученных соединений интеркаляции графита, KC 8, получают плавлением калия над графитовым порошком. Калий поглощается графитом, и материал меняет цвет с черного на бронзовый. Полученное твердое вещество является пирофорным. Состав объясняется предположением, что расстояние от калия до калия в два раза больше расстояния между шестиугольниками в углеродном каркасе. Связь между слоями анионного графита и катионами калия ионная. Электропроводность материала больше, чем у α-графита. KC 8 представляет собой сверхпроводник с очень низкой критической температурой T c = 0,14 К. Нагревание KC 8 приводит к образованию ряд продуктов разложения по мере удаления атомов K:
Через промежуточные соединения KC 24 ( синий цвет), KC 36, KC 48, в конечном итоге получается соединение KC 60.
Стехиометрия MC 8 наблюдается для M = K, Rb и Cs. Для более мелких ионов M = Li, Sr, Ba, Eu, Yb и Ca предельная стехиометрия составляет MC 6. Графит кальция CaC. 6получают путем погружения высокоориентированного пиролитического графита в жидкий сплав Li – Ca на 10 дней при 350 ° C. Кристаллическая структура CaC. 6принадлежит пространственной группе R3m. Расстояние между слоями графита увеличивается при интеркалировании Са с 3,35 до 4,524 Å, а расстояние углерод-углерод увеличивается с 1,42 до 1,444 Å.
 Структура CaC. 6
Структура CaC. 6С барием и аммиаком катионы сольватируются, что дает стехиометрию (Ba (NH 3)2,5 C 10,9 (стадия 1)) или с цезием, водородом и калием (CsC 8·K2H4/3 C8(стадия 1)).
В отличие от других щелочных металлов, количество интеркаляции Na очень мало. Квантово-механические расчеты показывают, что это происходит из довольно общего явления: среди щелочных и щелочноземельных металлов Na и Mg обычно имеют самая слабая химическая связь с данным субстратом по сравнению с другими элементами в той же группе периодической таблицы. Явление возникает из-за конкуренции между тенденциями в энергии ионизации и взаимодействием ион-субстрат в столбцах периодической таблицы. значительная интеркаляция Na в графит может происходить в тех случаях, когда ион заключен в оболочку растворителя в процессе соинтеркаляции. Сложная разновидность магния (I) также интеркалирована. в графит.
Соединения интеркалирования бисульфат графита и перхлорат графита могут быть получены обработкой графита сильными окислителями в присутствии сильных кислот. В отличие от графитов калия и кальция, углеродные слои окисляются в этом процессе: 48 C + 0,25 O 2 + 3 H 2SO4→ [C 24 ] [HSO 4 ] · 2H 2SO4+ 0,5 H 2O
В перхлорате графита плоские слои атомов углерода отстоят друг от друга на 794 пикометров и разделены ионами ClO 4. Катодное восстановление перхлората графита аналогично нагреванию KC 8, которое приводит к последовательному удалению HClO 4.
Как бисульфат графита, так и перхлорат графита являются лучшими проводниками по сравнению с графитом, как и прогнозируется при использовании положительного дырочный механизм. Реакция графита с [O 2 ] [AsF 6 ] дает соль [C 8 ] [AsF 6].
Ряд галогенидов металлов интеркалирует в графит. Наиболее изучены хлоридные производные. Примеры включают MCl 2 (M = Zn, Ni, Cu, Mn), MCl 3 (M = Al, Fe, Ga), MCl 4 (M = Zr, Pt) и т. Д. Материал состоит из слоев плотноупакованных слоев галогенидов металлов между листами углерода. Производное C ~ 8 FeCl 3 проявляет поведение спинового стекла. Эта система оказалась особенно плодородной для изучения фазовых переходов. Ступень n магнитного GIC имеет n графитовых слоев, разделяющих последовательные магнитные слои. По мере увеличения номера стадии взаимодействие между спинами в последовательных магнитных слоях становится слабее, и может возникнуть двумерное магнитное поведение.
Хлор и бром обратимо интеркалируют в графит. Йода нет. Фтор реагирует необратимо. В случае брома известны следующие стехиометрии: C n Br для n = 8, 12, 14, 16, 20 и 28.
Поскольку он образуется необратимо, монофторид углерода часто не классифицируется как интеркалирующее соединение. Он имеет формулу (CF) x. Его получают реакцией газообразного фтора с графитным углеродом при 215–230 ° C. Цвет сероватый, белый или желтый. Связь между атомами углерода и фтора ковалентная. Монофторид тетракарбона (C 4 F) получают обработкой графита смесью фтора и фтороводорода при комнатной температуре. Состав имеет черновато-синий цвет. Монофторид углерода не является электропроводным. Он был изучен в качестве материала катода в одном из типов первичных (неперезаряжаемых) литиевых батарей.
Оксид графита представляет собой нестабильное твердое вещество желтого цвета.
Соединения интеркалирования графита уже много лет очаровывают материаловедов благодаря своим разнообразным электронным и электрическим свойствам.
Среди сверхпроводящих соединений с интеркаляцией графита CaC. 6демонстрирует самую высокую критическую температуру T c = 11,5 К, которая дополнительно увеличивается при приложенном давлении (15,1 К. при 8 ГПа). Считается, что сверхпроводимость в этих соединениях связана с ролью межслоевого состояния, свободной электроноподобной зоны, расположенной примерно на 2 эВ (0,32 аДж) выше уровня Ферми ; сверхпроводимость возникает только при заполнении межслоевого состояния. Анализ чистого CaC. 6с использованием высококачественного ультрафиолетового света показал, что проводят измерения с помощью фотоэмиссионной спектроскопии с угловым разрешением. Открытие сверхпроводящей щели в полосе π * выявило существенный вклад в общую силу электрон-фононной связи за счет межзонного взаимодействия π * -слоев.
Бронза окрашенный материал KC 8 является одним из самых сильных известных восстановителей. Он также использовался в качестве катализатора в полимеризации и в качестве реагента сочетания для арилгалогенидов с бифенилов. В одном исследовании свежеприготовленный KC 8 обрабатывали 1-йодододеканом, доставляющим модификацию (углеродные пластинки размером микрометров с выступающими длинными алкильными цепями, обеспечивающими растворимость), которая растворима в хлороформ. Другое соединение графита калия, KC 24, было использовано в качестве монохроматора нейтронов. Новое важное применение для калиевого графита было представлено изобретением ионно-калийной батареи. Подобно литий-ионной батарее , в калий-ионной батарее вместо металлического анода следует использовать анод на основе углерода. В этом случае важным преимуществом является стабильная структура калиевого графита.
| На Викискладе есть материалы, относящиеся к соединениям интеркалирования графита. |