 Сульфид кадмия, прототип халькогенида металла, используется в качестве желтого пигмента.
Сульфид кадмия, прототип халькогенида металла, используется в качестве желтого пигмента.A халькогенид представляет собой химическое соединение, состоящее из по меньшей мере один халькоген анион и по меньшей мере еще один электроположительный элемент. Хотя все элементы группы 16 периодической таблицы определены как халькогены, термин халькогенид чаще используется для сульфидов, селенидов, теллуридов и полониды, а не оксиды. Многие металлические руды существуют в виде халькогенидов. Фотопроводящие халькогенидные стекла используются в ксерографии. Некоторые пигменты и катализаторы также созданы на основе халькогенидов. Дихалькогенид металла MoS 2 представляет собой обычную твердую смазку.
Монохалькогениды щелочных металлов и щелочноземельных металлов являются солеподобными, бесцветными и часто водорастворимыми. Сульфиды имеют тенденцию подвергаться гидролизу с образованием производных, содержащих анионы бисульфида 2 (SH). Халькогениды щелочных металлов часто кристаллизуются со структурой анти флюорита, а соли щелочноземельных металлов - в мотиве хлорида натрия.
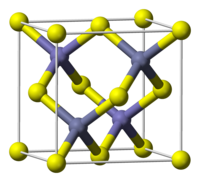 Структура цинковой обманки является распространенным мотивом для монохалькогенидов металлов.
Структура цинковой обманки является распространенным мотивом для монохалькогенидов металлов.Халькогениды переходных металлов встречаются со многими стехиометриями и многими структурами. Однако наиболее распространенными и наиболее технологически важными являются халькогениды простой стехиометрии, например 1: 1 и 1: 2. К крайним случаям относятся фазы, богатые металлами (например, Ta 2 S), которые демонстрируют обширную связь металл-металл, и материалы, богатые халькогенидами, такие как Re 2S7, которые обладают обширной связью халькоген-халькоген.
С целью классификации этих материалов халькогенид часто рассматривается как дианион, то есть S, Se, Te и Po. Фактически, халькогениды переходных металлов являются ковалентными, а не ионными, на что указывают их полупроводниковые свойства.
 Структура сульфида Nb с высоким содержанием металлов 21S8.
Структура сульфида Nb с высоким содержанием металлов 21S8.В большинстве своих халькогенидов переходные металлы принимают степень окисления II или выше. Тем не менее, существует несколько примеров, когда металлических атомов намного больше, чем халькогенов. Такие соединения обычно имеют обширную связь металл-металл.
Монохалькогениды металлов имеют формулу ME, где M = переходный металл и E = S, Se, Te. Обычно они кристаллизуются в одном из двух мотивов, названных в честь соответствующих форм сульфида цинка. В структуре цинковой обманки атомы сульфида упаковываются с кубической симметрией, а ионы Zn занимают половину тетраэдрических дырок. В результате получился каркас алмазоид. Основной альтернативной структурой для монохалькогенидов является структура вюрцита, в которой связи атомов одинаковы (тетраэдрические), но симметрия кристалла гексагональная. Третий мотив монохалькогенида металла представляет собой решетку арсенида никеля, в которой металл и халькогенид имеют октаэдрическую и тригонально-призматическую координацию соответственно. Этот мотив обычно подвержен нестехиометрии.
. Важные монохалькогениды включают некоторые пигменты, особенно сульфид кадмия. Многие минералы и руды являются моносульфидами.
Дихалькогениды металлов имеют формулу ME 2, где M = переходный металл, а E = S, Se, Te. Как правило, наиболее важными членами являются сульфиды. Они всегда представляют собой темные диамагнитные твердые вещества, нерастворимые во всех растворителях и проявляющие полупроводниковые свойства. С точки зрения их электронной структуры, эти соединения обычно рассматриваются как производные M, где M = Ti (d-конфигурация), V (d-конфигурация), Mo (d-конфигурация). Дисульфид титана был исследован в прототипе катодов для вторичных батарей, с использованием его способности обратимо претерпевать интеркалирование литием литием. Дисульфид молибдена, которому посвящены многие тысячи публикаций, является основной рудой молибдена, где его называют молибденитом. Он используется как твердый смазочный материал и катализатор для гидродесульфуризации. Соответствующие диселениды и даже дителлуриды известны, например, TiSe 2, MoSe 2 и WSe 2.
 MoS 2, наиболее распространенный дихалькогенид металлов, имеет слоистую структуру.
MoS 2, наиболее распространенный дихалькогенид металлов, имеет слоистую структуру.Дихалькогениды переходных металлов обычно имеют структуры либо дииодида кадмия, либо дисульфида молибдена. В мотиве CdI 2 металлы проявляют октаэдрические структуры. В мотиве MoS 2, который не наблюдается для дигалогенидов, металлы проявляют тригонально-призматические структуры. Сильная связь между металлическими и халькогенидными лигандами контрастирует со слабой халькогенид-халькогенидной связью между слоями. Благодаря такой разной прочности связи эти материалы вступают в интеркалирование щелочными металлами. Процесс интеркаляции сопровождается переносом заряда, в результате чего центры M (IV) восстанавливаются до M (III).
В отличие от классических дихалькогенидов металлов, железный пирит, обычный минерал, обычно описывается как состоящий из Fe и персульфидо-аниона S 2. Атомы серы в дисульфидодианионе связаны короткой связью S-S. «Поздние» дисульфиды переходных металлов (Mn, Fe, Co, Ni) почти всегда имеют мотив пирита или родственного марказита, в отличие от ранних металлов (V, Ti, Mo, W), которые имеют мотив 4+ степень окисления с двумя дианионами халькогенидов.
Некоторые металлы, в основном ранние металлы (группы Ti, V, Cr, Mn), также образуют трихалькогениды. Эти материалы обычно обозначаются как M (E 2) (E) (где E = S, Se, Te). Хорошо известным примером является триселенид ниобия. Аморфный MoS 3 получают обработкой тетратиомолибдата кислотой:
Минерал патронит, имеющий формулу VS 4, является примером тетрахалькогенида металла. Кристаллографический анализ показывает, что материал можно рассматривать как бис (персульфид), то есть V, (S 2)2.
 As2S3представляет собой сшитый полимер, где центры As и S подчиняются правило октетов.
As2S3представляет собой сшитый полимер, где центры As и S подчиняются правило октетов.Производные халькогена известны для всех элементов основной группы, кроме благородных газов. Обычно их стехиометрия соответствует классическим тенденциям валентности, например, SiS 2, B2S3, Sb2S3. Однако существует множество исключений., например, P4S3 и S4N4. Структуры многих материалов основной группы продиктованы направленной ковалентной связью, а не плотной упаковкой.
Халькогену приписываются положительные степени окисления для галогенидов, нитридов и оксидов.