 | |
| Имена | |
|---|---|
| Название ИЮПАК Гидрокарбонат кальция | |
| Другие имена Очищающая известь | |
| Идентификаторы | |
| 3D-модель (JSmol ) | |
| ChemSpider | |
| PubChem CID | |
| UNII | |
| Панель управления CompTox (EPA ) | |
InChI
| |
УЛЫБКИ
| |
| Свойства | |
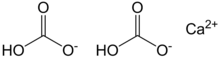
| Химические формула | Ca (HCO 3)2 |
| Молярная масса | 162,11464 г / моль |
| Растворимость в воде | 16,1 г / 100 мл (0 ° C). 16,6 г / 100 мл (20 ° C)). 18,4 г / 100 мл (100 ° C) |
| Опасности | |
| Основная га zards | Раздражающий |
| Температура вспышки | Невоспламеняющийся |
| Родственные соединения | |
| Прочие катионы | Бикарбонат магния |
| Если не указано иное, данные для материалов приведены в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки в ink | |
Бикарбонат кальция, также называемый гидрокарбонатом кальция, имеет химическую формулу Ca (HCO 3)2. Термин не относится к известному твердому соединению; он существует только в водном растворе, содержащем кальций (Ca), бикарбонат (HCO. 3) и карбонат (CO. 3) вместе с растворенным диоксидом углерода (CO 2). Относительные концентрации этих углеродсодержащих частиц зависят от pH ; бикарбонат преобладает в пределах 6,36–10,25 в пресной воде.
Все воды, контактирующие с атмосферой, поглощают углекислый газ, и когда эти воды вступают в контакт с горными породами и отложениями, они приобретают ионы металлов, чаще всего кальция и магния, поэтому большинство природных вод, которые поступающие из ручьев, озер и особенно колодцев, можно рассматривать как разбавленные растворы этих бикарбонатов. Эта жесткая вода имеет тенденцию к образованию карбонатной накипи в трубах и котлах, и они реагируют с мылом с образованием нежелательной пены.
Попытки получить соединения, такие как твердый бикарбонат кальция, путем выпаривания его раствора досуха неизменно дают вместо этого твердый карбонат кальция :
Очень мало твердых бикарбонатов, кроме таковых щелочных металлов, кроме известно, что существуют литий и ион аммония.
Указанная выше реакция очень важна для образования сталактитов, сталагмитов, колонны и другие образования внутри пещер и, если уж на то пошло, в формировании самих пещер. Когда вода, содержащая диоксид углерода (включая дополнительный CO 2 2 7, полученный из почвенных организмов), проходит через известняк или другие минералы, содержащие карбонат кальция, она растворяет часть карбоната кальция и, следовательно, становится богаче бикарбонатом. Когда грунтовые воды попадают в пещеру, избыток углекислого газа высвобождается из раствора бикарбоната, вызывая осаждение гораздо менее растворимого карбоната кальция.
В обратном процессе растворенный диоксид углерода (CO 2) в дождевой воде (H 2 O) реагирует с известняком кальцием. карбонат (CaCO 3) с образованием растворимого бикарбоната кальция (Ca (HCO 3)2). Это растворимое соединение затем вымывается дождевой водой. Эта форма выветривания называется карбонизацией.
В медицине бикарбонат кальция иногда вводят внутривенно для немедленной коррекции сердечных депрессорных эффектов гиперкалиемии за счет увеличения концентрации кальция в сыворотке и в то же время коррекции обычно присутствующей кислоты