 | |
| Клинические данные | |
|---|---|
| Торговые наименования | Мектови |
| Другие наименования | MEK162, ARRY-162, ARRY-438162 |
| AHFS / Drugs.com | Монография |
| MedlinePlus | a618041 |
| Данные лицензии |
|
| Класс препарата | Противоопухолевый Агенты |
| Код УВД | |
| Правовой статус | |
| Правовой статус |
|
| Идентификаторы | |
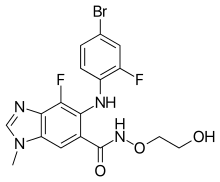
Название ИЮПАК
| |
| Номер CAS | |
| PubChem CID | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| KEGG | |
| ChEBI | |
| |
| CompTox Dashboard (EPA ) | |
| ECHA InfoCard | 100.167.617 |
| Химические и физические данные | |
| Формула | C17H15BrF 2N4O3 |
| Молярная масса | 441,233 г · моль |
| 3D-модель (JSmol ) | |
SMILES
| |
InChI
| |
Биниметиниб, также известный как Мектови и ARRY-162, является противораковым маленьким молекула, которая была разработана Array Biopharma для лечения различных видов рака. Биниметиниб является селективным ингибитором MEK, центральной киназы в способствующем опухоли пути MAPK. Было показано, что неправильная активация этого пути происходит при многих раковых заболеваниях. В июне 2018 года он был одобрен FDA в сочетании с энкорафенибом для лечения пациентов с неоперабельной или метастатической меланомой BRAF V600E или V600K с положительной мутацией.
Биниметиниб является пероральным ингибитором митоген-активируемой протеинкиназы киназы (MEK), или, более конкретно, Ингибитор MAP2K. MEK является частью пути RAS, который участвует в пролиферации и выживании клеток. МЭК активируется при многих формах рака. Биниметиниб, неконкурентоспособный с АТФ, связывается и ингибирует активность киназы MEK1 / 2, которая, как было показано, регулирует несколько ключевых клеточных активностей, включая пролиферацию, выживаемость и ангиогенез. MEK1 / 2 представляют собой треонин / тирозинкиназы с двойной специфичностью, которые играют ключевую роль в активации пути RAS / RAF / MEK / ERK и часто активируются в различных типах опухолевых клеток. Ингибирование MEK1 / 2 предотвращает активацию зависимых от MEK1 / 2 эффекторных белков и факторов транскрипции, что может привести к ингибированию передачи клеточных сигналов, опосредованной факторами роста. Как показали доклинические исследования, это может в конечном итоге привести к подавлению пролиферации опухолевых клеток и подавлению продукции различных воспалительных цитокинов, включая интерлейкин-1, -6 и фактор некроза опухоли.
В 2015 году он проходил III фазу клинических испытаний для рака яичников, мутантной меланомы BRAF и NRAS мутантной меланомы Q61.
В декабре 2015 года компания объявила об успешном исследовании меланомы мутантного NRAS. В ходе исследования у тех, кто получал биниметиниб, медиана выживаемости без прогрессирования составляла 2,8 месяца по сравнению с 1,5 месяцами для тех, кто получал стандартную терапию дакарбазином. NDA отправлено в июне 2016 г., и FDA должно принять решение к 30 июня 2017 года.
В апреле 2016 года было сообщено, что исследование фазы III рака яичников низкой степени злокачественности было прекращено из-за недостаточной эффективности.
Биниметиниб был изучен для лечения ревматоидного артрита, но исследование фазы II не показало положительных результатов.
В 2017 году FDA сообщило Array Biopharma, что данных исследования фазы III недостаточно и Заявка на новый препарат была отозвана.
В июне 2018 года он был одобрен для лечения некоторых меланом Управлением по контролю за продуктами и лекарствами США (FDA) в комбинации с энкорафенибом.. FDA одобрило биниметиниб в основном на основании данных одного клинического испытания (NCT01909453) с участием 383 пациентов с меланомой с положительной мутацией BRAF V600, которая была запущена или не могла быть удалена хирургическим путем. Исследование проводилось в 162 центрах в Европе, Северной Америке и различных странах по всему миру.