 | |
 | |
| Имена | |
|---|---|
| Название ИЮПАК хлорид самария (III) | |
| Другие названия трихлорид самария. трихлорсамарий | |
| Идентификаторы | |
| Номер CAS |
|
| 3D-модель (JSmol ) | |
| ChemSpider | |
| ECHA InfoCard | 100.030.712 |
| UNII | |
| CompTox Dashboard (EPA ) | |
InChI
| |
УЛЫБКИ
| |
| Свойства | |
| Химические формула | SmCl 3 |
| Молярная масса | 256,76 г / моль (безводный). 364,80 г / моль (гекса гидрат ) |
| Внешний вид | бледно-желтое твердое вещество (безводное) твердое вещество кремового цвета (гексагидрат) |
| Плотность | 4,46 г / см (anh водный) 2,383 г / см (гексагидрат) |
| Точка плавления | 682 ° C (1260 ° F; 955 K) |
| Температура кипения | разлагается |
| Растворимость в воде | 92,4 г / 100 мл (10 ° C ) |
| Структура | |
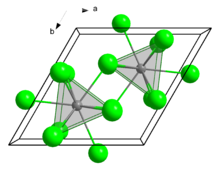
| Кристаллическая структура | гексагональный, hP8 |
| Пространственная группа | P63/ м, № 176 |
| Координационная геометрия | Трехугольный треугольный призматический элемент. (девять координат) |
| Опасности | |
| Основные опасности | Раздражающее |
| Родственные соединения | |
| Прочие анионы | Фторид самария (III). Бромид самария (III). Оксид самария (III) |
| Прочие катионы | хлорид самария (II). хлорид прометия (III). хлорид европия (III) |
| Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобокс | |
хлорид самария (III), также известный как трихлорид самария, представляет собой неорганическое соединение из самария и хлорида. Это бледно-желтая соль, которая быстро поглощает воду с образованием гекса гидрат, SmCl 36H2O. Соединение имеет мало практичных приложений, но используется в лабораториях для исследования новых соединений самария.
Подобно нескольким родственным хлоридам лантаноидов и актиноиды, SmCl 3 кристаллизуется в мотиве UCl 3. Центры Sm являются девятикоординатными, занимая тригональные призматические позиции с дополнительными хлоридными лигандами, занимающими три квадратные грани.
SmCl 3 получают способом «хлорид аммония », который включает начальный синтез (NH 4)2[SmCl 5 ]. Этот материал может быть получен из обычных исходных материалов при температуре реакции 230 ° C из оксида самария :
Затем пентахлорид нагревают до 350-400 ° C, что приводит к выделению хлорид аммония и оставив остаток безводного трихлорида:
Он также может быть получен из металлического самария и соляной кислоты.
Можно приготовить водные растворы хлорида самария (III) растворением металлического самария или карбоната самария в соляной кислоте.
Хлорид самария (III) представляет собой умеренно сильную кислоту Льюиса, которая считается «твердой» в соответствии с Концепция HSAB. Водный так Растворы хлорида самария могут быть использованы для получения трифторида самария :
Хлорид самария (III) используется для получения металла самарий, который имеет множество применений, особенно в магнитах. Безводный SmCl 3 смешивают с хлоридом натрия или хлоридом кальция с получением эвтектической смеси с низкой точкой плавления. Электролиз этого расплавленного солевого раствора дает свободный металл.
хлорид самария (III) также может быть использован в качестве отправной точки для получения других самариевые соли. Безводный хлорид используется для получения металлоорганических соединений самария, таких как комплексы бис (пентаметилциклопентадиенил) алкилсамария (III).