 | |
| Имена | |
|---|---|
| Название IUPAC (3S, 7R, 9S, 9aR) -5-Гидрокси-3,6,9-триметил-7- (2-метил-1-пропен-1-ил) -2,3,7,8,9,9a-гексагидро-1H-фенален-4- yl β- D -ксилопиранозид | |
| Идентификаторы | |
| 3D-модель (JSmol ) | |
| ChEMBL |
|
| ChemSpider | |
| PubChem CID | |
| UNII | |
InChI
| |
УЛЫБКА
| |
| Свойства | |
| Химическая формула | C25H36O6 |
| Молярная масса | 432,557 г · моль |
| За исключением случаев, когда в противном случае, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки ink | |
Псевдоптерозин A - это дитерпен гликозид, выделенный из морского кнута Pseudopterogorgia elisabethae, обнаруженного на Багамах и Флорида-Кис. Псевдоптерозины A-D, которые различаются степенью ацетилирования сахарного кольца, были впервые выделены и зарегистрированы в 1986 году. Из этого вида морских животных выделено по крайней мере 25 уникальных дитерпенов. Было обнаружено, что образцы P. elisabethae с Багамских островов имеют более высокие концентрации псевдоптерозинов, чем популяции из Флорида-Кис, которые имеют большее разнообразие дитерпеновых структур.
Псевдоптерозины обладают противовоспалительным действием. и анальгетическая активность с механизмом действия, отличным от обычных нестероидных противовоспалительных средств, НПВП. В коммерческих целях псевдоптерозины обнаруживаются в кремах для кожи в качестве местных противовоспалительных агентов.
Элизабетатриен (2 ) был определен как ключевой промежуточный продукт для синтеза класс псевдоптерозинов и секопсевдоптерозинов. Предлагаемый механистический путь синтеза элизабетатриена из геранилгеранилпирофосфата (GGPP, 1 ) описан ниже. Элизабетатриен-синтаза, фермент дитерпенциклаза, катализирует превращение дитерпенового GGPP в 10-членный углеродный скелет с последующей миграцией гидрида в направлении бициклической кольцевой системы. Этот фермент циклаза был идентифицирован как ключевой фермент в формировании углеродного скелета псевдоптерозинов за один этап. Был предложен альтернативный механизм, в котором сначала образуется шестичленное кольцо, а затем замыкается второе кольцо для бициклической системы.
 Циклизация GPP до элизабетатриена
Циклизация GPP до элизабетатриена Биосинтез псевдоптерозинов продолжается с ароматизацией до эрогиоргиена (3 ), два окисления до дигироксиэрогиоргиена (4, затем 5 ) и другое окисление до орто-гидроксихинона (6 ). Замыкание кольца (7 ), повторная ароматизация до (8 ) и гликозилирование дают псевдоптерозин A (9 ). Это вероятный путь биосинтеза, и промежуточные соединения 2, 3, 6, 7и 8 были идентифицированы с помощью исследований радиоактивного мечения. Был предложен альтернативный механизм без промежуточного гидроксихинона (6 ). Скорее, молекула 3 подвергается двум последующим окислениям по C-6 и C-7 до структуры, напоминающей 8, а затем гликозилированию до псевдоптерозина.
 Общая схема биосинтеза псевдоптерозина A
Общая схема биосинтеза псевдоптерозина A Точка разветвления для биосинтеза трициклических псевдоптерозинов по сравнению с бициклическими секопсевдоптерозинами происходит в соединении 11, ароматизированном велосипедном эрогиоргиаене. 11 окисляется один раз, затем гидроксилируется с последующим гликолсилированием с образованием бициклических секопсевдоптерозинов.
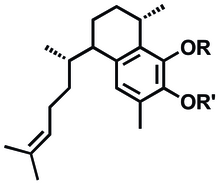 Общая структура секо-псевдоптерозинов
Общая структура секо-псевдоптерозинов Предлагаемый синтез искусственных противовоспалительных метаболитов смоделирован на основе псевдоптерозинов и основан на структуре бициклического секоптероптерозина 6.