| Синтез хинолина Knorr | |
|---|---|
| Названо в честь | Людвиг Кнорр |
| Тип реакции | Реакция образования кольца |
| Идентификаторы | |
| RSC ID онтологии | RXNO: 0000394 |
Синтез хинолина Кнорра представляет собой внутримолекулярная органическая реакция превращения β-кетоанилида в 2-гидроксихинолин с использованием серной кислоты. Эта реакция была впервые описана Людвигом Кнорром (1859–1921) в 1886 году.

Реакция представляет собой тип электрофильного ароматического замещения, сопровождаемого элиминированием воды.. Исследование 1964 года показало, что при определенных условиях реакции образование 4-гидроксихинолина является конкурирующей реакцией. Например, соединение бензоилацетанилид (1 ) образует 2-гидроксихинолин (2 ) в большом избытке полифосфорной кислоты (PPA), но 4-гидроксихинолин 3, когда количество PPA невелико. Механизм реакции идентифицировал N, O-дикатионный промежуточный продукт A с избытком кислоты, способный к замыканию цикла, и монокатионный промежуточный продукт B, который фрагментируется до анилина. и (в конечном итоге) ацетофенон. Анилин реагирует с другим эквивалентом бензоилацетанилида до образования 4-гидроксихинолина.

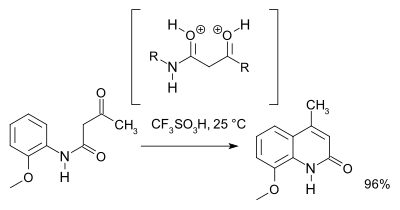
В исследовании 2007 года был пересмотрен механизм реакции, и на основе ЯМР-спектроскопии и теоретических расчетов предпочтение отдается O, O-дикатионному промежуточному соединению (суперэлектрофилу ) по сравнению с N, O-дикатионным промежуточным соединением. Для препаративных целей рекомендуется трифликовая кислота :