Контрольная точка иммунитета
редактировать

Контрольные точки иммунитета в микросреде опухоли

Контрольные точки иммунной иммуносупрессивной активности ассоциированные с раком груди
Иммунные контрольные точки являются регуляторами иммунной системы. Эти пути имеют решающее значение для самотолерантности, что предотвращает беспорядочную атаку иммунной системы клеток. Тем не менее, некоторые виды рака могут защитить себя от атак, стимулируя иммунные контрольные точки.
Ингибирующие молекулы контрольных точек являются мишенями для иммунотерапии рака из-за их возможности использования при различных типах рака. В настоящее время одобренные ингибиторы контрольных точек блок CTLA4 и PD-1 и PD-L1. За соответствующие открытия в фундаментальной науке Джеймс П. Эллисон и Тасуку Хондзё получили премию Танга в области биофармацевтики и Нобелевскую премию по физиологии и медицине. в 2018 г.
Содержание
- 1 Стимулирующие молекулы контрольных точек
- 2 Ингибирующие молекулы контрольных точек
- 3 Ингибиторы иммунных контрольных точек
- 4 Ссылки
Стимулирующие молекулы контрольных точек
Четыре стимулирующих молекулы контрольной точки являются членами суперсемейства рецепторов фактора некроза опухоли (TNF) - CD27, CD40, OX40, GITR и CD137. Еще две молекулы стимулирующих контрольных точек относятся к суперсемейству B7-CD28 - собственно CD28 и ICOS.
- CD27 : эта молекула поддерживает антиген-специфическую экспансию наивных Т-клеток и жизненно важна для генерации Т-клеточной памяти. CD27 также является маркером памяти В-клеток. Активность CD27 регулируется временной доступностью его лиганда, CD70, на лимфоцитах и дендритных клетках. Известно, что костимуляция CD27 подавляет функцию эффекторных клеток Th17. Американская биотехнологическая компания Celldex Therapeutics работает над CDX-1127, агонистическим анти-CD27 моноклональным антителом, которое на животных моделях показало свою эффективность в контексте стимуляции Т-клеточного рецептора.
- CD28 : эта молекула конститутивно экспрессируется почти на всех CD4 + T-клетках человека и примерно на половине всех CD8 T-клеток. Связывание с двумя его лигандами: CD80 и CD86, экспрессируемыми на дендритных клетках, вызывает экспансию Т-клеток. CD28 был мишенью TGN1412 «суперагониста», который вызвал тяжелые воспалительные реакции в первом исследовании на людях в Лондоне в марте 2006 года.
- CD40 : эта молекула, обнаруженная в различных клеток иммунной системы, включая антигенпрезентирующие клетки, имеет CD40L, иначе известный как CD154, и временно экспрессируется на поверхности активированных CD4 + Т-клеток в качестве лиганда. Известно, что передача сигнала CD40 «лицензирует» дендритные клетки на созревание и тем самым запускает активацию и дифференцировку Т-клеток. В 2012 году ныне несуществующая биотехнологическая компания из Сиэтла под названием VLST получила лицензию на моноклональное антитело к агонисту CD40 у Pfizer. Швейцарская фармацевтическая компания Roche приобрела этот проект после закрытия VLST вниз в 2013 г.
- CD122 : известно, что эта молекула, которая является субъединицей рецептора интерлейкина-2 бета, увеличивает пролиферацию эффекторных Т-клеток CD8 +. Американская биотехнологическая компания Nektar Therapeutics работает над NKTR-214, результатами Фазы I иммуностимулирующего цитокина с смещением по CD122, объявленными в ноябре 2016 года.
- CD137 : Когда эта молекула, также называемая 4 -1BB, связывается лигандом CD137, результатом является пролиферация Т-клеток. Также известно, что передача сигналов, опосредованная CD137, защищает Т-клетки и, в частности, CD8 + Т-клетки от гибели клеток, вызванной активацией. Немецкая биотехнологическая компания Pieris Pharmaceuticals разработала сконструированный липокалин, который является биспецифичным в отношении CD137 и HER2.
- OX40 : эта молекула, также называемая CD134, имеет OX40L или CD252, в качестве его лиганда. Подобно CD27, OX40 способствует размножению эффекторных Т-клеток и Т-клеток памяти, однако он также известен своей способностью подавлять дифференцировку и активность Т-регуляторных клеток, а также регуляцией продукции цитокинов. Значение OX40 как лекарственной мишени в первую очередь заключается в том, что, будучи временно экспрессируемым после взаимодействия с Т-клеточным рецептором, он активируется только на самых недавно активированных антигеном Т-клетках в воспалительных поражениях. Было показано, что моноклональные антитела против OX40 имеют клиническое применение при запущенном раке. Фармацевтическая компания AstraZeneca разрабатывает три препарата, нацеленных на OX40: MEDI0562 - гуманизированный агонист OX40; MEDI6469, мышиный агонист OX4; и MEDI6383, агонист OX40
- GITR : сокращение от гена, индуцированного глюкокортикоидами семейства TNFR, вызывает экспансию Т-клеток, включая экспансию Treg. Лиганд для GITR в основном экспрессируется на антигенпрезентирующих клетках. Было показано, что антитела к GITR способствуют противоопухолевому ответу за счет потери стабильности линии Treg. Биотехнологическая компания TG Therapeutics работает над антителами против GITR
- ICOS : эта молекула, сокращенно от Inducible T-cell costimulator, также называемая CD278, экспрессируется на активированных T-клетках. Его лиганд - ICOSL, экспрессируется в основном на В-клетках и дендритных клетках. Молекула, по-видимому, играет важную роль в эффекторной функции Т-клеток. Американская биотехнологическая компания Jounce Therapeutics разрабатывает агонист ICOS.
Ингибирующие молекулы контрольной точки
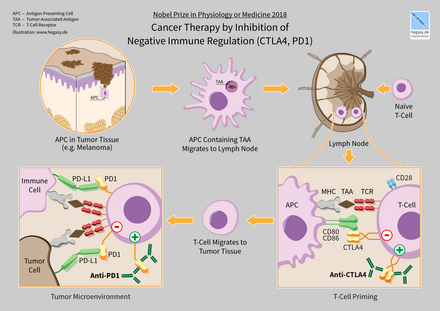
Терапия рака путем ингибирования негативной иммунной регуляции (CTLA4, PD1)
- A2AR : рецептор аденозина A2A считается важная контрольная точка в терапии рака, потому что аденозин в иммунном микроокружении, ведущий к активации рецептора A2a, представляет собой петлю отрицательной иммунной обратной связи, а в опухолевом микроокружении относительно высокие концентрации аденозина.
- B7-H3 : также называется CD276 Первоначально считалось, что это костимуляторная молекула, но теперь рассматривается как ко-ингибирующая. Американская биотехнологическая компания MacroGenics работает над MGA271 - Fc-оптимизированным моноклональным антителом, нацеленным на B7-H3. Рецепторы B7-H3 еще не идентифицированы.
- B7-H4 : также называется VTCN1, экспрессируется опухолевыми клетками и ассоциированными с опухолью макрофагами и играет роль в ускользании от опухоли.
- BTLA : Эта молекула, сокращение от B и T Lymphocyte Attenuator и также называемая CD272, имеет HVEM (Herpesvirus Entry Mediator) в качестве лиганда. Поверхностная экспрессия BTLA постепенно снижается во время дифференциации человеческих CD8 + Т-клеток от фенотипа наивных до эффекторных клеток, однако опухолеспецифические человеческие CD8 + Т-клетки экспрессируют высокие уровни BTLA.
- CTLA-4 : сокращение от Cytotoxic T -Лимфоцит-ассоциированный белок 4, также называемый CD152, является целью препарата для лечения меланомы Yervoy Bristol-Myers Squibb, который получил одобрение FDA в марте 2011 года. Экспрессия CTLA-4 на Treg-клетках служит для контроля Пролиферация Т-клеток.
- IDO : сокращение от индолеамин-2,3-диоксигеназа, представляет собой катаболический фермент триптофана с иммуно-ингибирующими свойствами. Другой важной молекулой является ТДО, триптофан-2,3-диоксигеназа. IDO, как известно, подавляет T- и NK-клетки, генерирует и активирует Treg и миелоидные супрессорные клетки и способствует ангиогенезу опухоли.
- KIR : сокращение от Killer-cell Immunoglobulin-like Receptor, является рецептором для Молекулы MHC Class I на Natural Killer cells. Bristol-Myers Squibb работает над Lirilumab, моноклональным антителом к KIR.
- LAG3 : сокращение от Lymphocyte Activation Gene-3, работает для подавления иммунного ответа посредством действия на Tregs, а также прямого воздействия на CD8 + T-клетки. Bristol-Myers Squibb находится в фазе I с моноклональным антителом против LAG3 под названием BMS-986016.
- NOX2 : сокращение от никотинамидадениндинуклеотидфосфата изоформа 2 НАДФН оксидазы, представляет собой фермент миелоидные клетки, которые генерируют иммуносупрессивные активные формы кислорода. Генетическое и фармакологическое ингибирование NOX2 в миелоидных клетках улучшает противоопухолевые функции соседних NK-клеток и Т-клеток, а также запускает аутоиммунитет у людей и экспериментальных животных. NOX2 является целью Цеплена, который получил одобрение для использования при остром миелоидном лейкозе в рамках EU.
- PD-1 : сокращение от Programmed Death 1 (PD-1) рецептор имеет два лиганда, PD-L1 и PD-L2. Этот контрольно-пропускной пункт является целью препарата Кейтруда, выпускаемого компанией Merck Co. для лечения меланомы, который получил одобрение FDA в сентябре 2014 года. Контрольно-пропускной пункт также является целью препарата Bavencio EMD Serono (Merck KGaA), который получил одобрение FDA в 2017 году. Преимущество нацеливания на PD-1 заключается в том, что он может восстанавливать иммунную функцию в микроокружении опухоли.
- TIM-3 : сокращение от Т-клеточного домена иммуноглобулина и домена 3 муцина, экспрессируется на активированных CD4 + Т-клетках человека и регулирует Th1 и цитокины Th17. TIM-3 действует как негативный регулятор функции Th1 / Tc1, вызывая гибель клеток при взаимодействии с его лигандом, галектин-9.
- VISTA : сокращение от V-домена Ig супрессор активации Т-клеток, VISTA в первую очередь экспрессируется на гемопоэтических клетках, так что последовательная экспрессия VISTA на лейкоцитах в опухолях может позволить блокаде VISTA быть эффективной в широком диапазоне солидных опухолей.
- SIGLEC7 (лектин 7 иммуноглобулинового типа, связывающийся с сиаловой кислотой, также обозначены как CD328) и SIGLEC9 (лектин 9 иммуноглобулинового типа, связывающийся с сиаловой кислотой, также обозначаемый как CD329) представляют собой белки, обнаруженные на поверхности различных иммунных клеток, включая естественные клетки-киллеры и макрофаги (SIGLEC7 ) и нейтрофилов, макрофагов, дендритных клеток и активированных Т-клеток (SIGLEC9 ). SIGLEC 7 и 9 подавляют иммунную функцию этих клеток, связываясь с терминальной сиаловой кислотой на гликанах, покрывающих поверхность клеток.
Ингибиторы иммунных контрольных точек
Лекарства или лекарственные препараты-кандидаты, которые ингибируют / блокируют молекулы ингибирующих контрольных точек иногда называют ингибиторами контрольных точек ; эту идею часто называют блокадой иммунных контрольных точек или просто блокадой контрольных точек. Фармацевтические исследования лекарств с ингибиторами контрольных точек увеличиваются в компаниях, включая Bristol-Myers Squibb, Merck, Merck KGaA, Roche и AstraZeneca. Palleon Pharmaceuticals разрабатывает новую область препаратов-ингибиторов контрольных точек, которые работают над ингибированием SIGLEC 7 и SIGLEC 9 как нового класса рецепторов для терапевтических средств с использованием антител.
Ссылки
 Контрольные точки иммунитета в микросреде опухоли
Контрольные точки иммунитета в микросреде опухоли  Контрольные точки иммунной иммуносупрессивной активности ассоциированные с раком груди
Контрольные точки иммунной иммуносупрессивной активности ассоциированные с раком груди  Терапия рака путем ингибирования негативной иммунной регуляции (CTLA4, PD1)
Терапия рака путем ингибирования негативной иммунной регуляции (CTLA4, PD1)