 | |
| Клинические данные | |
|---|---|
| Торговые наименования | Xcopri |
| Другие названия | YKP3089 |
| AHFS / Drugs.com | xcopri |
| Пути. введения | Устно |
| Правовой статус | |
| Правовой статус |
|
| Идентификаторы | |
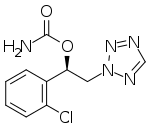
Название ИЮПАК
| |
| Номер CAS | |
| PubChem CID | |
| PubChem SID | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| KEGG | |
| ChEMBL |
|
| Химические и физические данные | |
| Формула | C10H10ClN 5O2 |
| Молярная масса | 267,67 г · моль |
| 3D-модель (JSmol ) | |
УЛЫБКИ
| |
InChI
| |
сенобамат, продается под торговой маркой Xcopr i - это лекарство, используемое для лечения приступов с частичным началом у взрослых.
Он был одобрен для медицинского применения в США в ноябре 2019 года и помещен в Список V в марте 2020 года.
Ценобамат является блокатором потенциал-управляемых натриевых каналов (VGSC) . Он является селективным блокатором инактивированного состояния VGSC, предпочтительно ингибируя постоянный ток натрия. Было высказано предположение, что ценобамат дополнительно усиливает пресинаптическое высвобождение γ-аминомасляной кислоты (ГАМК), тем самым увеличивая ингибирующее ГАМКергическое действие. нейротрансмиссия.
Безопасность и эффективность ценобамата для лечения приступов с частичным началом были установлены в двух рандомизированных двойных слепых плацебо-контролируемых исследованиях, в которых приняли участие 655 взрослых. В этих исследованиях пациенты имели приступы с частичным началом с вторичной генерализацией или без нее в среднем в течение примерно 24 лет, а средняя частота приступов составляла 8,5 приступов за 28 дней в течение 8-недельного исходного периода. Во время испытаний дозы 100, 200 и 400 миллиграммов (мг) в день снижали процент приступов за 28 дней по сравнению с группой плацебо. Рекомендуемая поддерживающая доза после периода титрования (корректировки приема лекарств) составляет 200 мг в день; однако некоторым пациентам может потребоваться дополнительное титрование до 400 мг в день, максимальной рекомендованной дозы, в зависимости от их клинического ответа и переносимости.
Ценобамат одобрен Управлением по контролю за продуктами и лекарствами США (FDA) в ноябре 2019 г. и удовлетворил заявку на Xcopri в SK Life Science Inc.