 | |
 | |
| Идентификаторы | |
|---|---|
| Номер CAS | |
| 3D-модель (JSmol ) | |
| ChemSpider | |
InChI
| |
УЛЫБКИ
| |
| Свойства | |
| Химическая формула | XeOF 4 |
| Молярная масса | 223,23 г / моль |
| Внешний вид | бесцветная жидкость |
| Плотность | 3,17 г / см, жидкость |
| Точка плавления | - 46,2 ° C (-51,2 ° F; 227,0 K) |
| Растворимость в воде | Реагирует с водой |
| Структура | |
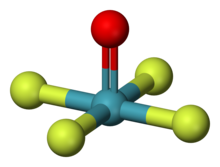
| Молекулярная форма | квадратно-пирамидальная |
| Если не указано иное, данные приведены для материалы в их стандартной статистике e (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки ink | |
Ксенон окситетрафторид (Xe O F 4) является неорганическое химическое соединение. Это бесцветная стабильная жидкость с температурой плавления -46,2 ° C, которую можно синтезировать частичным гидролизом XeF. 6 или реакцией XeF. 6с диоксидом кремния или <39.>NaNO. 3 :
Синтез с высоким выходом протекает по реакции XeF. 6с POF. 3 при - 196 ° C.
Как и большинство оксидов ксенона, он чрезвычайно реакционноспособен и нестабилен и гидролизуется в воде с образованием опасно опасных и коррозионных продуктов, включая фтористый водород :
Кроме того, образуются также некоторое количество озона и фтора. Эта реакция чрезвычайно опасна, поэтому окситетрафторид ксенона следует хранить вдали от любых следов воды или водяного пара при любых условиях.
XeOF 4 реагирует с H 2 O в следующих этапах:
Образовавшийся XeO 3 представляет собой опасное взрывчатое вещество, взрывчатое разлагающееся на Xe и O 2:
В жидкой форме XeOF. 4проявляет амфотерное поведение, образуя комплексы как с сильными основаниями Льюиса, такими как CsF, так и с сильными кислотами Льюиса, такими как SbF. 5. Он образует аддукт 1: 1 с XeF. 2, изоструктурный с XeF. 2· IF. 5, а также с различными фторидами тяжелых щелочных металлов.
Реакция XeOF. 4с XeO. 3 обеспечивает удобный маршрут синтеза для.