 | |
 | |
| Имена | |
|---|---|
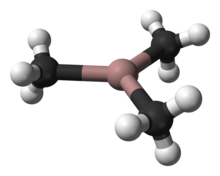
| Название ИЮПАК триметилгаллан, триметанидогаллий | |
| Идентификаторы | |
| Номер CAS | |
| 3D-модель (JSmol ) | |
| ChemSpider | |
| ECHA InfoCard | 100.014.452 |
| PubChem CID | |
| CompTox Dashboard (EPA ) | |
InChI
| |
УЛЫБКА
| |
| Свойства | |
| Химическая формула | Ga (CH 3)3 |
| Молярная масса | 114,827 г / моль |
| Внешний вид | прозрачная бесцветная жидкость |
| Точка плавления | -15 ° C (5 ° F; 258 K) |
| Точка кипения | 55,7 ° C (132,3 ° F; 328,8 K) |
| Опасности | |
| Основные опасности | пирофорные |
| Если не указано иное, данные приведены для материалы в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на ink | |
Триметилгаллий, часто сокращенно TMG или TMGa, представляет собой галлиевоорганическое соединение формулы Ga (CH 3)3. Это бесцветная пирофорная жидкость. В отличие от триметилалюминия, но аналогично триметилиндию, TMG является мономерным.
TMG получают реакцией трихлорида галлия с различными метилирующими агентами. К ним относятся метиллитий, диметилцинк и триметилалюминий. Менее летучий аддукт диэтилового эфира можно получить, используя метилмагний иодид в эфире. Эфирные лиганды также могут быть замещены жидким аммиаком.
TMG является предпочтительным металлооргом органический источник галлия для металлоорганической парофазной эпитаксии (MOVPE) галлийсодержащих сложных полупроводников, таких как GaAs, GaN, GaP, GaSb, InGaAs, InGaN, AlGaInP, InGaP и AlInGaNP. Этот материал используется в производстве светодиодного освещения и полупроводников в качестве предшественника химического осаждения металлоорганических соединений из паровой фазы.