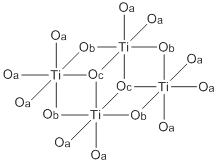
 . Сокращенная структура этоксида титана (IV). Этоксидные лиганды обозначены буквами О. Концевые этоксидные лиганды обозначены Oa, двояковыпуклые лиганды обозначены Ob, а трехкомпонентные лиганды обозначены Oc. . Сокращенная структура этоксида титана (IV). Этоксидные лиганды обозначены буквами О. Концевые этоксидные лиганды обозначены Oa, двояковыпуклые лиганды обозначены Ob, а трехкомпонентные лиганды обозначены Oc. | |
| Названия | |
|---|---|
| Название IUPAC этанолат; титан (4+) | |
| Систематическое наименование IUPAC тетраэтанолат титана (4+) | |
| Другие названия Этилтитанат, тетраэтилтитанат | |
| Идентификаторы | |
| Номер CAS | |
| 3D-модель (JSmol ) | |
| ChemSpider | |
| ECHA InfoCard | 100.019.464 |
| Номер EC |
|
| PubChem CID | |
| UNII | |
| CompTox Dashboard (EPA ) | |
InChI
| |
УЛЫБКА
| |
| Свойства | |
| Химическая формула | C32H80O16Ti4 |
| Молярная масса | 228,109 г / моль |
| Внешний вид | бесцветная жидкость |
| Плотность | 1,088 |
| Точка кипения | 150–152 (@ 10 мм рт. Ст.) |
| Если не указано иное, данные для материалов приведены в их стандарте состояние (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки в ink | |
Этоксид титана - это химическое соединение с формулой Ti4(ОСН 2CH3)16. Это цвет меньше жидкости, которая растворяется в органических растворителях, но легко гидролизуется. Он продается как бесцветный раствор. Алкоксиды титана (IV) и циркония (IV) используются в органическом синтезе и материаловедении. Они принимают более сложные структуры, чем предполагают их эмпирические формулы.
Этоксид титана получают обработкой тетрахлорида титана этанолом в присутствии амина:
Чистота этоксида титана составляет обычно анализируется протонной ЯМР спектроскопией. Ti (OEt) 4 1H ЯМР (90 МГц, хлороформ-d, м.д.): 4,36 (квартет, 8H, CH602), 1,27 (триплет, 12H, CH169>Структура
Оба Ti (OEt) 4 существуют в основном в виде тетрамеров с октаэдрическим координационным окружением вокруг металлических центров. Существует два типа титановых центров, в зависимости от количества концевых или мостиковых алкоксидов. лиганды. Zr (OEt) 4 имеет сходную структуру. Виртуальная симметрия основной структуры M 4O16для тетрамерных структур этих соединений - C 2h.
Подобно этоксиду, метоксид титана Ti (OMe) 4 существует в виде тетрамера с каждым из металлических центров Ti, имеющим октаэдрическое координационное окружение.
Что касается объемных алкильных групп, Ti (OPr) 4, напротив, существует как мономер с тетраэдрическим окружением вокруг центра Ti. Эта более низкая степень координации с металлическим центром объясняется стерической массой группы Pr по сравнению с н-алкильными группами, это служит для предотвращения мостиковых взаимодействий между металлическими центрами.
Этоксид циркония может быть получен способом, аналогичным, но не идентичным соединению титана:
Более распространенным способом синтеза этоксида циркония является обработка тетрахлорида циркония желаемым спиртом и аммиаком:
Этоксид циркония можно также получить с дихлоридом цирконоцена:
Zr (OPr) 4 также имеет структуру этоксида титана.
Алкоксиды Ti и Zr могут использоваться для осаждения микроструктурированных пленок TiO 2 или ZrO 2:
Эти пленки образуются в результате гидролиза из алкоксид на поверхности раздела. Важно отметить, что TiO 2 и ZrO 2, образованные в результате этих реакций, имеют полимерную структуру, благодаря чему их можно использовать в качестве гидроизоляционных, устойчивых к царапинам или термостойких покрытий. На структуру пленок оксидов металлов, выращенных в этом веществе, влияет присутствие основных или кислотных катализаторов гидролиза. Обычно кислотный катализ дает золь, в котором полимерные цепи ориентированы случайным образом и линейны. В случае, опосредованном основанием, образуются густые кластеры или сшитые сети, эти структуры могут улавливать растворитель и побочные продукты реакции и образовывать гелевое покрытие. Алкоксиды Ti и Zr также являются потенциальными исходными материалами для катализаторов Циглера-Натта, используемых в полимеризации алкена.