 | |
 | |
 | |
| Имена | |
|---|---|
| Имена ИЮПАК Тетрахлорид циркония. Хлорид циркония (IV) | |
| Идентификаторы | |
| Номер CAS | |
| 3D-модель (JSmol ) | |
| ChEBI | |
| ChemSpider | |
| ECHA InfoCard | 100.030.041 |
| Номер EC |
|
| PubChem CID | |
| UNII | |
| Панель управления CompTox (EPA ) | |
InChI
| |
УЛЫБКИ
| |
| Свойства | |
| Химическая формула | ZrCl 4 |
| Молярная масса | 233,04 г / моль |
| Внешний вид | белые кристаллы. гигроскопичны |
| Плотность | 2,80 г / см |
| Температура плавления | 437 ° C (819 ° F; 710 K) (тройная точка) |
| Температура кипения | 331 ° C (628 ° F, 604 K) (сублимируется) |
| Solub Способность в воде | гидролиз |
| Растворимость | концентрированная HCl (с реакцией) |
| Структура | |
| Кристаллическая структура | Моноклинная, mP10 |
| Пространственная группа | P12 / c1, No. 13 |
| Термохимия | |
| Теплоемкость (C) | 125,38 ДжК моль |
| Стандартная молярная. энтропия (S 298) | 181,41 ДжК моль |
| Стандартная энтальпия образования. (ΔfH298) | −980,52 кДж / моль |
| Опасности | |
| Паспорт безопасности | MSDS |
| NFPA 704 (огненный алмаз) |  0 3 2 0 3 2 |
| Температура вспышки | Невоспламеняющийся |
| Смертельная доза или концентрация (LD, LC): | |
| LD50(средняя доза ) | 1688 мг / кг (перорально, крыса). 655 мг / кг (мышь, перорально) |
| Другие анионы | Фторид циркония (IV). Бромид циркония (IV). Йодид циркония (IV) |
| Другое катионы | тетрахлорид титана. тетрахлорид гафния |
| родственные соединения | , хлорид циркония (III) |
| Если не указано иное, данные приводятся для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |
| Infobo x ссылки | |
хлорид циркония (IV), также известный как тетрахлорид циркония, (Zr Cl 4) представляет собой неорганическое соединение, часто используемое в качестве предшественника других соединений цирконий. Это белое тугоплавкое твердое вещество быстро гидролизуется во влажном воздухе.
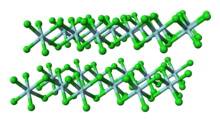
В отличие от молекулярного TiCl 4, твердый ZrCl 4 имеет полимерную структуру, в которой каждый Zr имеет октаэдрическую координацию. Это различие в структурах является причиной несоответствия в их свойствах: TiCl. 4пригоден для дистилляции, а ZrCl. 4- твердое вещество. В твердом состоянии ZrCl 4 принимает ленточноподобную линейную полимерную структуру - такую же структуру, как и HfCl 4. Этот полимер легко разлагается при обработке основаниями Льюиса, которые расщепляют связи Zr-Cl-Zr.
Это превращение влечет за собой обработку оксида углеродом в качестве оксидный «геттер» и хлор.
В процессе лабораторного масштаба используется четыреххлористый углерод вместо углерода и хлора:
ZrCl 4 является промежуточным продуктом при превращении минералов циркония в металлический цирконий по процессу Кролла. В природе минералы циркония неизменно существуют в виде оксидов (что также отражено в тенденции всех хлоридов циркония к гидролизу). Для преобразования в объемный металл эти тугоплавкие оксиды сначала превращаются в тетрахлорид, который можно перегонять при высоких температурах. Очищенный ZrCl 4 может быть восстановлен металлическим Zr с получением хлорида циркония (III).
ZrCl 4 является наиболее распространенным прекурсором для химического осаждения из паровой фазы диоксида циркония и диборида циркония.
В органическом синтезе тетрахлорид циркония используется в качестве слабой кислоты Льюиса для Реакция Фриделя-Крафтса, реакция Дильса-Альдера и реакции внутримолекулярной циклизации. Он также используется для водоотталкивающей обработки текстиля и других волокнистых материалов.
Гидролиз ZrCl 4 дает гидратированный гидроксихлоридный кластер, называемый цирконилхлорид. Эта реакция протекает быстро и практически необратимо, что соответствует высокой оксофильности циркония (IV). По этой причине манипуляции с ZrCl 4 обычно требуют безвоздушных методов..
ZrCl 4 является основным исходным соединением для синтеза многих металлоорганических комплексов циркония. Из-за своей полимерной структуры ZrCl 4 обычно превращается в молекулярный комплекс перед использованием. Он образует комплекс 1: 2 с тетрагидрофураном : CAS [21959-01-3], т.пл. 175–177 ° C. NaC 5H5взаимодействует с ZrCl 4 (THF) 2 с образованием дихлорида цирконоцена, ZrCl 2(C5H5)2, универсального циркониевого комплекса. Одним из наиболее любопытных свойств ZrCl 4 является его высокая растворимость в присутствии метилированных бензолов, таких как дурен. Эта солюбилизация происходит за счет образования π-комплексов.
Логарифм (по основанию 10) давления пара тетрахлорида циркония (от 480 до 689 К) определяется уравнением: log 10 (P) = -5400 / T + 11,766, где давление измеряется в торр, а температура - в кельвинах. Логарифм (основание 10) давления пара твердого тетрахлорида циркония (от 710 до 741 K) определяется уравнением log 10 (P) = -3427 / T + 9.088. Давление при температуре плавления составляет 14 500 торр.
| На Wikimedia Commons есть носители, связанные с хлоридом циркония (IV). |