 | |
 | |
 | |
| Имена | |
|---|---|
| Название IUPAC Олово (II) оксид | |
| Другие названия Оксид олова, оксид олова | |
| Идентификаторы | |
| Номер CAS | |
| 3D-модель (JSmol ) | |
| ECHA InfoCard | 100.040.439 |
| Номер EC |
|
| PubChem CID | |
| Номер RTECS |
|
| UNII | |
| Панель управления CompTox (EPA ) | |
InChI
| |
SMILES
| |
| Свойства | |
| Химическая формула | SnO |
| Молярная масса | 134,709 г / моль |
| Внешний вид | черный или красный порошок в безводном состоянии, белый в гидратированном состоянии |
| Плотность | 6,45 г / см |
| Точка плавления | 1080 ° C (1980 ° F; 1350 K) |
| Растворимость в воде | нерастворимый |
| Магнитная восприимчивость (χ) | -19,0 · 10 см / моль |
| Структура | |
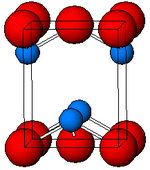
| Кристаллическая структура | тетрагональная |
| Термохимия | |
| Стандартная молярная. энтропия (S 298) | 56 Дж · моль · K |
| Стандартная энталь py. образования (ΔfH298) | -285 кДж · моль |
| Опасности | |
| Паспорт безопасности | ICSC 0956 |
| Температура вспышки | Невоспламеняющийся |
| NIOSH (пределы воздействия на здоровье в США): | |
| PEL (допустимое) | нет |
| REL (рекомендуется) | TWA 2 мг / м |
| IDLH (Непосредственная опасность) | ND |
| Родственные соединения | |
| Прочие анионы | Сульфид олова. Селенид олова. Теллурид олова |
| Прочие катионы | Окись углерода. Монооксид кремния. Оксид германия (II). Оксид свинца (II) |
| Родственные олова оксиды | Диоксид олова |
| Если не указано иное, данные представлены дано для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на ink | |
Оксид олова (II) (оксид двухвалентного олова ) представляет собой соединение формулы SnO. Он состоит из олова и кислорода, где олово имеет степень окисления +2. Есть две формы: стабильная сине-черная форма и метастабильная красная форма.
 Горение оксида олова (II)
Горение оксида олова (II) Сине-черный SnO может быть полученный нагреванием гидрата оксида олова (II), SnO · xH 2 O (x <1) осаждается, когда соль олова (II) взаимодействует с гидроксидом щелочного металла, таким как NaOH.. Метастабильный, красный SnO может быть получен путем осторожного нагревания осадка, образовавшегося при воздействии водного раствора аммиака на соль олова (II).. SnO может быть получен в виде чистого вещества в лаборатории путем контролируемого нагревания оксалата олова (II). (оксалат двухвалентного олова) в отсутствие воздуха или в атмосфере CO 2. Этот метод также применяется для производства оксида железа и оксида марганца.
Оксид олова (II) горит на воздухе тусклым зеленым пламенем с образованием SnO 2.
При нагревании в инертной атмосфере первоначально происходит диспропорционирование с образованием металлического Sn и Sn 3O4, который в дальнейшем реагирует с образованием SnO 2 и металлического Sn.
SnO является амфотерным, растворяется в сильной кислоте с образованием солей олова (II) и в сильном основании с образованием станнитов, содержащих Sn (OH) 3. Его можно растворить в сильнокислых растворах с образованием ионных комплексов Sn (OH 2)3и Sn (OH) (OH 2)2), а в менее кислых растворах - с образованием Sn 3 (OH) 4. Обратите внимание, что безводные станниты, например K 2Sn2O3, K 2 SnO 2, также известны. SnO является восстановителем и, как считается, восстанавливает медь (I) к металлическим кластерам при производстве так называемого «медно-рубинового стекла».
Черный, α-SnO принимает структуру тетрагонального слоя PbO, содержащего четыре координаты квадратные пирамидальные атомы олова. Эта форма встречается в природе как редкий минерал. Асимметрию обычно приписывают стерически активной неподеленной паре; однако расчеты электронной плотности показывают, что асимметрия вызвана разрыхляющим взаимодействием Sn (5s) и O (2p) -орбитали.
В SnO наблюдалась нестехиометрия.
Электронная запрещенная зона была измерена между 2,5 эВ и 3 эВ.
Оксид двухвалентного олова в основном используется в качестве прекурсора в производстве. кольцо других, обычно трехвалентных, соединений или солей олова. Оксид двухвалентного олова также можно использовать в качестве восстановителя и при создании рубинового стекла. Он редко используется в качестве катализатора этерификации .
Оксид церия (III) в форме керамики вместе с оксидом олова (II) (SnO) используется для освещения УФ-светом.